抗菌药物是一类能够抑制细菌、真菌等病原微生物生长繁殖或直接杀灭病原微生物的化学物质,如抗生素、抗菌肽(antimicrobial peptides, AMPs)等[1-2]。自1928年英国科学家弗莱明(Alexander Fleming)发现第一个抗生素—青霉素以来,抗生素被广泛应用于疾病的防治中,挽救了无数的生命。起初,抗生素是一种被用作治疗细菌感染的药物,然而近年来抗菌药物的超标使用、无节制滥用,导致细菌耐药性问题日益严重。技术迭代缓慢致使新药研发困难,细菌产生耐药的速度远超过新抗菌药物研发速度,抗菌药物尤其是抗生素领域的专利申请数量在2011年后呈现下降的趋势[3],世界范围内即将面临重症细菌感染无药可用的境地。因此,合理使用现有抗菌药物,提升抗菌药物的利用效率,抑制细菌耐药性的发展迫在眉睫。本文就不同抗菌药物的抗菌机制,以及细菌产生耐药性的特点,重点介绍极具抗生素替代潜质的AMPs与传统抗菌药物联合抗菌的策略。该策略作为一种新的治疗耐药细菌感染和减少细菌耐药性产生的有效方法,发挥协同增效的抗菌作用,降低单个抗菌药物的用量,创新AMPs应用策略,为解决传统抗菌药物耐药性问题提供新方向。
1 抗菌药物的抗菌机制抗菌药物的抗菌机制主要有以下4种:抑制细菌细胞壁的形成,破坏细胞膜结构,干扰细菌内DNA的复制、转录及翻译,破坏蛋白质合成。值得注意的是,抗菌药物不仅可以通过其中某一种机制发挥抗菌作用,也可以通过多种机制相结合的方式发挥抗菌效力[4]。
根据细菌种类不同细菌的细胞壁成分主要包括肽聚糖、脂多糖及磷壁酸等,是许多抗菌药物作用的靶点。抗菌药物能够导致细胞壁成分生物合成机制发生故障,出现合成和降解的无效循环,从而诱导细胞调亡[5-7]。细胞壁内侧的细胞膜是保护细胞内环境的重要屏障。人们普遍认为,AMPs主要通过破坏细胞膜结构,使细胞膜上形成孔道,致使细胞溶解,从而杀灭病原微生物[8-11]。目前已发现的AMPs破膜机制主要包括“桶板”“毯式”“环孔”等模式,如阳离子AMPs首先与呈负电性的细胞膜结合,随后AMPs通过不同模式透化细菌细胞膜,影响细菌细胞内的生命活动[12],见图 1。
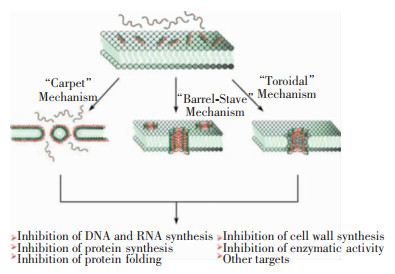 |
| 图 1 阳离子AMPs与细胞膜的相互作用示意图[12] |
在DNA复制过程中,DNA拓扑异构酶催化DNA链的断裂与结合,影响DNA链的拓扑状态。旋转酶和拓扑异构酶IV作为DNA复制过程中最重要的两个拓扑异构酶,是抗菌药物常见靶点[13-14]。目前DNA聚合酶也是研究较为广泛的药物潜在靶点[15-16]。此外,抗菌药物可以通过与RNA聚合酶结合,干扰细菌DNA转录及RNA延伸,起到杀菌作用[17]。部分抗菌药物还能够通过干扰蛋白质合成起始阶段、肽链的延伸、氨基酸代谢等发挥抗菌功能[18]。某些富含脯氨酸的AMPs可以被细菌的特殊转运载体经主动运输到细胞内特定靶点,与70S核糖体相互作用进而破坏蛋白质合成,达到杀灭细菌的目的[19-20]。
2 细菌耐药性的产生耐药的发生是细菌在持续抗菌药物作用下,感受自身所处的不良环境条件而产生的防御机制。细菌通过细胞膜通透性改变,主动外排泵系统过表达,作用靶点结构改变,抗菌药物的破坏与修饰,以及携带外源性耐药基因等方式对抗菌药物产生耐药性,如图 2所示[21]。
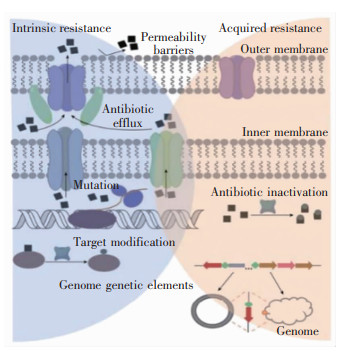 |
| 图 2 内在及获得性耐药机制示意图[21] |
细胞膜的通透性以及抗菌药物进入细胞的能力是决定药物疗效的关键性因素,一些细菌细胞膜通道或细胞壁孔道的改变,使得抗菌药物不易进入菌体,进而产生耐药性[22-23]。药物外排泵在细菌中普遍存在,不仅能减少抗菌药物在细菌细胞内的积累,还为细菌提供了足够的时间适应不同药物,进入菌体的药物在外排泵作用下迅速排出,菌体细胞内药物浓度降低,耐药性随之产生[24-26]。药物靶点结构的改变则会降低药物与靶点的亲和力,进而导致抗菌药物活性减弱或失活,是细菌产生耐药性的另一重要机制[18, 27-28]。此外,抗菌药物在发挥作用的过程中其本身也可能被降解或发生结构改变,该过程往往有酶的参与。一方面,蛋白酶的水解作用导致对酶敏感的抗菌药物的关键反应中心被破坏或发生不易逆转的结构重排;另一方面,抗菌药物的共价修饰阻碍药物与其靶点的相互作用,从而导致耐药的产生[29]。
如果仅依靠上述耐药机制,细菌的多重耐药(multidrug resistance, MDR)不易在短时间内暴发。此外,细菌还通过偶联、转化或转导获得携带耐药基因的DNA元件,以水平基因转移(horizontal gene transfer, HGT)的方式从其他细菌中获得外源性耐药基因,整合入自身基因组而产生MDR[30-31]。
3 联合用药协同抗菌由于细菌耐药性的持续发展,致使很多严重的临床细菌感染使用现有抗菌药物很难达到理想的治疗效果,而新药研发缓慢,成本较高,推广困难,且同样存在引发耐药性的风险。因此,基于不同抗菌药物对细菌抗菌机制不同而进行联合用药,有望成为对抗细菌耐药性的新策略。此策略能够将现有抗菌药物进行再利用,使抗菌效果最大化,避免新药研发的巨额费用。与单一抗菌药物相比,抗菌药物联用具有多靶点的抗菌作用方式,能够有效杀灭耐药菌株,并抑制细菌耐药性的发展。
3.1 协同抗菌机制目前,学者们主要集中于以下四种协同抗菌机制的研究:增强抗菌药物的渗透性,抑制共同的生化途径,抑制细菌内某些保护性酶的产生,以及细胞壁活性剂的组合。其中,对增强抗菌药物的渗透性报道最广泛,此机制主要是基于其中一个抗菌药物对细菌细胞膜通透性及功能的影响,使另一个抗菌药物进入细胞的效率升高或抑制细胞膜上外排泵对抗菌药物的外排作用,进而提高细胞内抗菌药物的浓度,提升抗菌效果。AMPs与抗菌药物的联用多采用此机制发挥协同抗菌作用。AMPs可以改变细菌细胞膜的通透性,促进抗菌药物进入细菌细胞,作用于细胞内靶点[32],见图 3。除此之外,两种不同的抗菌药物能够通过共同抑制某一生化途径,如蛋白质合成等而增强抗菌作用。最近研究[33-34]表明,具有抗炎和抗氧化作用的双氢青蒿素与头孢呋辛能够协同抑制蛋白质生成。许多细菌还能够产生不同种类的保护性酶如β-内酰胺酶,能够水解青霉素等作用于细菌细胞壁的β-内酰胺类抗生素,导致此类抗生素作用效果不佳。β-内酰胺酶抑制剂可抑制耐药菌内β-内酰胺酶产生,故临床上常将β-内酰胺酶抑制剂如relebactam与β-内酰胺类抗生素联用,以有效保护抗生素不被水解,进而使抗生素抗菌作用发挥至最大[35]。作用于细菌细胞壁的化合物除β-内酰胺类抗生素外,还有糖肽类、磷霉素等[36]。2022年研究[37]发现,同为细胞壁活性剂的亚胺培南与磷霉素联用能够通过干扰细胞壁代谢产生协同作用。
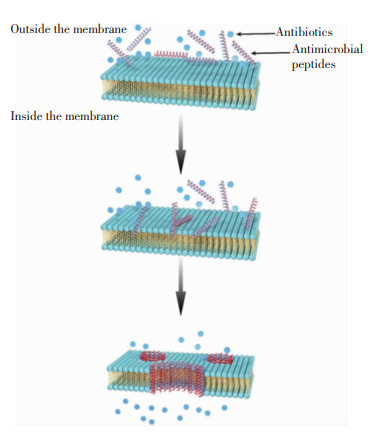 |
| 图 3 AMPs与抗菌药物联用发挥协同抗菌作用的示意图[32] |
除单一细菌自身能够对抗菌药物产生耐药性外,细菌黏附于物体表面,通过分泌多糖等物质使彼此聚集在一起并进一步增殖,最终形成致密的具有屏障作用的生物膜,抵抗抗菌药物的作用,使得细菌的耐药性大幅度提高。因此,有学者将对细菌生物膜具有高度破坏作用的抗菌药物与其他不具有生物膜破坏作用或破坏作用较小的抗菌药物联用,以期能够发挥协同抗菌活性。已有研究[38]发现,AMPs能够破坏细菌生物膜,当AMPs与抗菌药物联合使用时,AMPs的抗生物膜特性能够提高抗菌药物的抗菌效果。
3.2 传统抗菌药物的联合应用传统方法的单一抗菌药物治疗细菌感染很容易引起耐药,而抗菌药物联合应用,即同时使用两种或两种以上的抗菌药物,通过作用于多个靶点,从而提高抗菌效果,延缓耐药性的发展,是目前对现有传统抗菌药物再利用的有效方式。
抗菌药物的协同抗菌活性可通过棋盘法测定联合用药时抗菌药物的最低抑菌浓度计算部分抑菌浓度指数(fractional inhibitory concentration index, FIC index)来评价,当FIC index≤0.5时,判定为协同作用;当0.5<FIC index<4时,判定为无相互作用;当FIC index≥4时,判定为拮抗作用[39]。笔者前期研究发现,将妥布霉素与特殊官能团连接,设计获得的两亲性妥布霉素衍生物可以显著提高利福平或二甲胺四环素对多重耐药铜绿假单胞菌的抗菌活性,表现出极强的协同抗菌作用,其FIC index达到0.039[40-41]。两者的协同机制研究[40-41]发现,两亲性妥布霉素衍生物能够影响细胞膜上呼吸链的电子传递进而降低ATP的生成,抑制细胞膜上抗菌药物外排泵的功能,进而发挥协同抗菌作用。细菌细胞膜上抗菌药物外排泵的过表达是很多细菌产生耐药性的主要机制之一,目前研究的抗菌药物外排泵抑制剂如1-(1-萘甲基)哌嗪等能够恢复某些革兰阴性菌对抗菌药物的敏感性,但对于通过细胞壁屏障作用产生内源耐药性的细菌有效性大大降低。因此,增强细胞膜通透性同时降低抗菌药物外排泵功能是解决此问题的理想策略。本课题组将妥布霉素作为载体,与1-(1-萘甲基)哌嗪等不同外排泵抑制剂相连,获得了一系列化合物,该化合物与传统抗菌药物联合应用,显著提高了氟喹诺酮类抗菌药物环丙沙星、莫西沙星对耐药性铜绿假单胞菌的抗菌活性[42-43]。
金黄色葡萄球菌是一种革兰阳性球形细菌,能够引起局部感染甚至危及生命,万古霉素和环丙沙星等常被用于治疗金黄色葡萄球菌感染。为避免单独使用这些抗菌药物在治疗过程中可能引发的耐药性问题,Kamble等[44]提出联合使用不同抗菌药物,将达托霉素和万古霉素这类针对细胞结构的抗生素与另一种作用于DNA复制或蛋白质合成过程的抗菌药物如环丙沙星或妥布霉素两两组合;所有组合均显示出协同效应,并以剂量依赖的方式抑制和破坏生物膜。由此可见,这些传统抗菌药物联合使用比单独使用两者中任何一种药物更为有效,并有望缓解细菌耐药问题。
3.3 AMPs与传统抗菌药物联合应用MDR菌的出现以及随后使用传统抗菌药物治疗的失败,助推了新型抗菌药物的研发。AMPs作为生物体天然免疫系统的组成部分,鉴于其广谱的抗菌活性、无残留、无污染等特点,被认为具有开发为新型抗菌药物替代抗生素的潜质。更重要的是,普遍认为AMPs通过破坏细菌的细胞膜结构完整性发挥抗菌作用,此种抑菌方式不易引发耐药性,同时也为联合用药研究提供了理论基础。目前,关于AMPs与传统抗菌药物联合使用的研究已有诸多报道,且普遍认为二者的协同抗菌机制是AMPs对细菌细胞膜的破坏作用,致使细胞内抗菌药物浓度升高。本课题前期研究发现,具有细菌细胞膜破坏活性的AMPs与多种抗菌药物联用能够提高抗菌活性,且对临床分离的耐药菌株也具有较好的抗菌活性[45-46]。如富含脯氨酸的脂肽C12-PRP在与二甲胺四环素或利福平联合应用时,可显著提高二者对MDR和广谱耐药铜绿假单胞菌的抗菌活性,脂肽C12-PRP具有进一步开发为抗菌药物佐剂的潜质[47]。此外,有研究[48-49]发现,AMPs与同样作用于细菌细胞膜的抗菌药物联合应用时也可以产生协同抗菌效果。Field等[49]研究发现,AMPs Nisin与抗生素多黏菌素E联合应用时,AMPs Nisin大幅降低多黏菌素E抑制细菌生物膜所需的药物浓度,提高抗生素的抗菌效率和细菌对抗生素的敏感性。Jahangiri等[48]研究表明,AMPs Nisin和多黏菌素E联合应用对广谱耐药型鲍曼不动杆菌和多黏菌素E耐药性铜绿假单胞菌均表现出协同抗菌活性。
部分AMPs存在一定细胞毒性且易被蛋白酶水解,也是制约其在临床中应用的又一重要原因[50]。目前,为了最大限度地提高AMPs对不同细胞的选择性,一些研究试图通过序列修饰、肽链杂合和氨基酸替代等方法对AMPs进行修饰或改造。AamAP1-lysine是以蝎毒中发现的AMPs AamAP1作为基础设计获得的一种合成肽衍生物,其与左氧氟沙星、氯霉素、利福平、红霉素联合应用时,对金黄色葡萄球菌和铜绿假单胞菌表现出不同程度的协同抗菌作用,且在一些组合中AamAP1-lysine的最小抑菌浓度甚至从3 μmol/L降低至0.01 μmol/L[51]。Almaaytah等[51]对AamAP1-lysine与利福平联用的抗生物膜活性研究中,测得FIC index低至0.058,表现出强协同作用。Duan等[52]研究也发现,来源于斑马鱼的AMPs衍生肽Pt5-1c与抗生素联用后促进抗生素进入细菌细胞,从而对MDR菌产生协同抗菌效应以及抗生物膜效应。
3.4 AMPs与其他化合物的协同抗菌作用除传统抗菌药物外,某些AMPs与其他化合物也可产生协同抗菌作用。如蜂源AMPs Melittin是一种研究比较透彻的水溶性好、系统毒性高的AMPs。Melittin能够破坏细菌细胞膜,具有强抗菌活性[53]。孙楠等[54]研究发现,Melittin与柠檬酸联合应用时对大肠埃希菌、肠炎沙门菌及金黄色葡萄球菌均显示出协同抗菌效应,当与乙酸联合应用时对肠炎沙门菌表现为协同抗菌作用。微生物源AMPs是由微生物分泌的用来保护自身并杀灭或抑制其他微生物的小分子多肽,通常具有广谱抗菌活性,如利用侧孢短芽孢杆菌产生的AMPs Brevilaterin[55-56]。宁亚维等[57]研究证实,Brevilaterin与柠檬酸两者协同抑制大肠埃希菌的生长,破坏细菌细胞膜的完整性,导致细胞变形、DNA降解及细胞内容物泄漏。柠檬酸能够有效抑制有机酸的降解,延缓食物腐败,同时Brevilaterin与柠檬酸联合应用降低了单个抗菌药物的使用量,有望在食品保鲜中推广应用[58]。
4 AMPs与传统抗菌药物联合应用进展 4.1 食品防腐AMPs用作防腐剂,具有热稳定性好、安全无毒、抗菌性强等优点,因此在食品的防腐和保鲜中具有广阔的应用前景。AMPs Nisin在人体内不会长期积累,毒性小,作为食品防腐剂具有很高的安全性,且在某些地区已经被批准在食品贮藏中使用。Mirhoseini等[59]研究发现,Nisin与氧化镁纳米颗粒具有协同抗菌效应,应用于牛奶的杀菌灭活中,能够降低牛奶中大肠埃希菌和金黄色葡萄球菌的菌群数量。Nisin与香芹酚的联用同样能抑制牛奶中细菌繁殖,有望成为奶制品的保鲜策略[60]。此外,Li等[61]将β-环糊精与Nisin联合应用,有效提高了Nisin在胰蛋白酶中的稳定性,延缓Nisin的降解,显著抑制低熟猪肉中细菌的生长繁殖,使猪肉保持原有营养价值和独特的风味。
4.2 医药卫生目前,由MDR菌引起的医院获得性感染严重危害公共卫生安全,迫切需要研发新的抗菌策略攻克细菌耐药性。AMPs具有多种生物学功能,在先天免疫系统中发挥重要作用[62]。在AMPs临床应用策略创新研究中,Salouti等[63]发现,当AMPs MBP-1与银纳米粒子联合使用时,显著降低金黄色葡萄球菌的定植率,提高伤口愈合率。抗菌药物联合应用在体内的协同抗菌活性也得到证实。张馨元等[64]研究发现,AMPs LL-37和酰胺酶联合使用抑制感染粪肠球菌小鼠体内脏器中细菌的增殖,减轻脏器病理损伤。探索其协同机制发现,酰胺酶先破坏细菌细胞壁,有利于AMPs LL-37接触到细菌细胞膜,LL-37不仅能破坏细胞膜结构引起菌体细胞内容物外泄,还能够与细胞内的蛋白质、核酸相结合,影响细胞的生命活动,两机制相辅相成有效提高对粪肠球菌的杀伤效率。与此同时,该方法降低酰胺酶的使用量,抑制细菌耐药性的产生。最近研究[65]发现,LL-37与万古霉素、阿奇霉素、多黏菌素等抗生素联合使用有望成为治疗铜绿假单胞菌感染的新策略。此外,AMPs LP-23、DP-23和SPO与庆大霉素联用对临床分离的耐庆大霉素的大肠埃希菌表现出协同抗菌作用,进一步证实了AMPs与抗菌药物联用在治疗耐药菌株引起的细菌感染方面具有很大潜力[66]。
4.3 动物养殖在动物养殖中,AMPs可用于改善动物健康状况,促进动物生长,提高生长性能[67]。王莉等[68]研究证实,天蚕素和β-甘露聚糖酶对鹌鹑的生长有协同促进作用,一种合理的解释是β-甘露聚糖酶可降解甘露聚糖成为甘露寡糖,而甘露寡糖和AMPs均可刺激机体免疫系统细胞,减少肠道有害菌,提高日增重,降低料肉比。在肉鸡日粮中联合添加天蚕素和合生素改善了肉鸡小肠黏膜结构,促进小肠黏膜免疫细胞增殖[69]。另一个被广泛研究的猪源AMPs PR-39与阿莫西林、土霉素、硫酸链霉素联合应用,针对畜禽常见病原菌表现出明显协同抗菌作用[70]。
5 小结与展望细菌出于自我保护的原因对现有抗菌药物产生耐药,且随着细菌耐药的不断发展对人类健康的威胁日益加剧。本文综述基于不同抗菌机制的抗菌药物联合应用是在不开发新药的前提下,最经济高效的抑制细菌耐药性,治疗临床细菌感染的策略之一。在诸多抗菌药物联合应用研究中,AMPs与传统抗菌药物协同抗菌成为了研究热点,且有望攻克细菌耐药性。但抗菌药物联合应用对于不同细菌的最佳组合、临床抗菌效果,以及是否仍存在引发耐药性的风险等问题仍需深入研究,以期抗菌药物协同抗菌策略在食品、医疗、畜牧等领域得到更广泛的应用。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Li DW, Zhou B, Lv B. Antibacterial therapeutic agents composed of functional biological molecules[J]. J Chem, 2020, 2020: 6578579. |
| [2] |
Wang Y, Sun H. Polymeric nanomaterials for efficient delivery of antimicrobial agents[J]. Pharmaceutics, 2021, 13(12): 2108. DOI:10.3390/pharmaceutics13122108 |
| [3] |
赵蕴华, 刘沛然, 从俊杰. 全球新型抗生素专利技术及市场研究[J]. 情报工程, 2016, 2(6): 85-93. Zhao YH, Liu PR, Cong JJ. Research on the global new antibiotics patent technology and market[J]. Technology Intelligence Engineering, 2016, 2(6): 85-93. |
| [4] |
Lai ZH, Tan P, Zhu YJ, et al. Highly stabilized α-Helical coiled coils kill Gram-negative bacteria by multicomplementary mechanisms under acidic condition[J]. ACS Appl Mater Interfaces, 2019, 11(25): 22113-22128. DOI:10.1021/acsami.9b04654 |
| [5] |
Aerts R, Herrebout W, Johannessen C. Raman optical activity of the antibiotic vancomycin bound to its biological target[J]. J Raman Spectrosc, 2022, 53(7): 1220-1226. DOI:10.1002/jrs.6347 |
| [6] |
Lobritz MA, Andrews IW, Braff D, et al. Increased energy demand from anabolic-catabolic processes drives β-lactam antibiotic lethality[J]. Cell Chem Biol, 2022, 29(2): 276-286.e4. DOI:10.1016/j.chembiol.2021.12.010 |
| [7] |
Shi YN, Li YF, Yang K, et al. A novel milk-derived peptide effectively inhibits Staphylococcus aureus: interferes with cell wall synthesis, peptidoglycan biosynthesis disruption reaction mechanism, and its application in real milk system[J]. Food Control, 2023, 144: 109374. DOI:10.1016/j.foodcont.2022.109374 |
| [8] |
Lyu YF, Yang CY, Chen TT, et al. Characterization of an antibacterial dodecapeptide from pig as a potential food preservative and its antibacterial mechanism[J]. Food Funct, 2020, 11(5): 4090-4102. DOI:10.1039/D0FO00380H |
| [9] |
Lyu YF, Chen TT, Shang L, et al. Design of trp-rich dodecapeptides with broad-spectrum antimicrobial potency and membrane-disruptive mechanism[J]. J Med Chem, 2019, 62(15): 6941-6957. DOI:10.1021/acs.jmedchem.9b00288 |
| [10] |
Lai ZH, Jian Q, Li GY, et al. Self-assembling peptide dendron nanoparticles with high stability and a multimodal antimicrobial mechanism of action[J]. ACS Nano, 2021, 15(10): 15824-15840. DOI:10.1021/acsnano.1c03301 |
| [11] |
Chen TT, Lyu YF, Tan MS, et al. Fabrication of supramolecular antibacterial nanofibers with membrane-disruptive mechanism[J]. J Med Chem, 2021, 64(22): 16480-16496. DOI:10.1021/acs.jmedchem.1c00829 |
| [12] |
Huang YB, Huang JF, Chen YX. Alpha-helical cationic antimicrobial peptides: relationships of structure and function[J]. Protein Cell, 2010, 1(2): 143-152. DOI:10.1007/s13238-010-0004-3 |
| [13] |
Sanyal G, Doig P. Bacterial DNA replication enzymes as targets for antibacterial drug discovery[J]. Expert Opin Drug Discov, 2012, 7(4): 327-339. DOI:10.1517/17460441.2012.660478 |
| [14] |
Zhang J, Battini N, Ou JM, et al. New efforts toward amino-thiazolylquinolones with multitargeting antibacterial potential[J]. J Agric Food Chem, 2023, 71(5): 2322-2332. DOI:10.1021/acs.jafc.2c08293 |
| [15] |
Santos JA, Lamers MH. Novel antibiotics targeting bacterial replicative DNA polymerases[J]. Antibiotics (Basel), 2020, 9(11): 776. DOI:10.3390/antibiotics9110776 |
| [16] |
Tangadanchu VKR, Sui YF, Zhou CH. Isatin-derived azoles as new potential antimicrobial agents: design, synthesis and biological evaluation[J]. Bioorg Med Chem Lett, 2021, 41: 128030. DOI:10.1016/j.bmcl.2021.128030 |
| [17] |
Panayiotakopoulos GD, Papadimitriou DT. Rifampicin for COVID -19[J]. World J Virol, 2022, 11(2): 90-97. DOI:10.5501/wjv.v11.i2.90 |
| [18] |
Foster TJ. Antibiotic resistance in Staphylococcus aureus. Current status and future prospects[J]. FEMS Microbiol Rev, 2017, 41(3): 430-449. DOI:10.1093/femsre/fux007 |
| [19] |
Mishra AK, Choi J, Moon E, et al. Tryptophan-rich and proline-rich antimicrobial peptides[J]. Molecules, 2018, 23(4): 815. DOI:10.3390/molecules23040815 |
| [20] |
Peng SJ, Yang MY, Sun RN, et al. Mechanism of actions of oncocin, a proline-rich antimicrobial peptide, in early elongation revealed by single-molecule FRET[J]. Protein Cell, 2018, 9(10): 890-895. DOI:10.1007/s13238-017-0495-2 |
| [21] |
沙国萌, 陈冠军, 陈彤, 等. 抗生素耐药性的研究进展与控制策略[J]. 微生物学通报, 2020, 47(10): 3369-3379. Sha GM, Chen GJ, Chen T, et al. Strategies for controlling antibiotic resistance: a review[J]. Microbiology China, 2020, 47(10): 3369-3379. DOI:10.13344/j.microbiol.china.200668 |
| [22] |
Fajardo-Lubián A, Ben Zakour NL, Agyekum A, et al. Host adaptation and convergent evolution increases antibiotic resis-tance without loss of virulence in a major human pathogen[J]. PLoS Pathog, 2019, 15(3): e1007218. DOI:10.1371/journal.ppat.1007218 |
| [23] |
Khalid A, Lubián AF, Ma L, et al. Characterizing the role of porin mutations in susceptibility of beta lactamase producing Klebsiella pneumoniae isolates to ceftaroline and ceftaroline-avibactam[J]. Int J Infect Dis, 2020, 93: 252-257. DOI:10.1016/j.ijid.2020.02.005 |
| [24] |
Varela MF, Stephen J, Lekshmi M, et al. Bacterial resistance to antimicrobial agents[J]. Antibiotics (Basel), 2021, 10(5): 593. DOI:10.3390/antibiotics10050593 |
| [25] |
Manrique PD, López CA, Gnanakaran S, et al. New understanding of multidrug efflux and permeation in antibiotic resis-tance, persistence, and heteroresistance[J]. Ann N Y Acad Sci, 2023, 1519(1): 46-62. DOI:10.1111/nyas.14921 |
| [26] |
Grosjean M, Tazrout S, Bour M, et al. Reassessment of the cooperativity between efflux system MexAB-OprM and cephalosporinase AmpC in the resistance of Pseudomonas aeruginosa to β-lactams[J]. J Antimicrob Chemother, 2021, 76(2): 536-539. DOI:10.1093/jac/dkaa462 |
| [27] |
Qiao JJ, Zhu MJ, Lu ZX, et al. The antibiotics resistance mechanism and pathogenicity of cold stressed Staphylococcus aureus[J]. LWT, 2020, 126: 109274. DOI:10.1016/j.lwt.2020.109274 |
| [28] |
Liu JQ, Xiao G, Zhou WP, et al. Various novel colistin resis-tance mechanisms interact to facilitate adaptation of Aeromonas hydrophila to complex colistin environments[J]. Antimicrob Agents Chemother, 2021, 65(7): e0007121. DOI:10.1128/AAC.00071-21 |
| [29] |
Christaki E, Marcou M, Tofarides A. Antimicrobial resistance in bacteria: mechanisms, evolution, and persistence[J]. J Mol Evol, 2020, 88(1): 26-40. DOI:10.1007/s00239-019-09914-3 |
| [30] |
Le Roux F, Blokesch M. Eco-evolutionary dynamics linked to horizontal gene transfer in vibrios[J]. Annu Rev Microbiol, 2018, 72: 89-110. DOI:10.1146/annurev-micro-090817-062148 |
| [31] |
Sun DC, Jeannot K, Xiao YH, et al. Editorial: horizontal gene transfer mediated bacterial antibiotic resistance[J]. Front Microbiol, 2019, 10: 1933. DOI:10.3389/fmicb.2019.01933 |
| [32] |
Zhu YY, Hao WJ, Wang X, et al. Antimicrobial peptides, conventional antibiotics, and their synergistic utility for the treatment of drug-resistant infections[J]. Med Res Rev, 2022, 42(4): 1377-1422. DOI:10.1002/med.21879 |
| [33] |
黄梅, 罗俊, 沈建英. 双氢青蒿素与头孢呋辛对大肠杆菌的协同抗菌作用及机制研究[J]. 中国中药杂志, 2020, 45(12): 2975-2981. Huang M, Luo J, Shen JY. Synergistic antibacterial effect and mechanisms of dihydroartemisinin and cefuroxime incombination[J]. China Journal of Chinese Materia Medica, 2020, 45(12): 2975-2981. DOI:10.19540/j.cnki.cjcmm.20200225.402 |
| [34] |
Li JB, Bai YS, Ma KD, et al. Dihydroartemisinin alleviates deoxynivalenol induced liver apoptosis and inflammation in piglets[J]. Ecotoxicol Environ Saf, 2022, 241: 113811. DOI:10.1016/j.ecoenv.2022.113811 |
| [35] |
Lob SH, Karlowsky JA, Young K, et al. Activity of imipe-nem/relebactam against MDR Pseudomonas aeruginosa in Europe: SMART 2015-17[J]. J Antimicrob Chemother, 2019, 74(8): 2284-2288. DOI:10.1093/jac/dkz191 |
| [36] |
Sarkar P, Yarlagadda V, Ghosh C, et al. A review on cell wall synthesis inhibitors with an emphasis on glycopeptide antibiotics[J]. Medchemcomm, 2017, 8(3): 516-533. DOI:10.1039/C6MD00585C |
| [37] |
Singkham-In U, Chatsuwan T. Synergism of imipenem with fosfomycin associated with the active cell wall recycling and heteroresistance in Acinetobacter calcoaceticus-baumannii complex[J]. Sci Rep, 2022, 12(1): 230. DOI:10.1038/s41598-021-04303-7 |
| [38] |
Verderosa AD, Totsika M, Fairfull-Smith KE. Bacterial biofilm eradication agents: a current review[J]. Front Chem, 2019, 7: 824. DOI:10.3389/fchem.2019.00824 |
| [39] |
Odds FC. Synergy, antagonism, and what the chequerboard puts between them[J]. J Antimicrob Chemother, 2003, 52(1): 1. DOI:10.1093/jac/dkg301 |
| [40] |
Lyu YF, Yang X, Goswami S, et al. Amphiphilic tobramycin-lysine conjugates sensitize multidrug resistant Gram-negative bacteria to rifampicin and minocycline[J]. J Med Chem, 2017, 60(9): 3684-3702. DOI:10.1021/acs.jmedchem.6b01742 |
| [41] |
Lyu YF, Domalaon R, Yang X, et al. Amphiphilic lysine conjugated to tobramycin synergizes legacy antibiotics against wild-type and multidrug-resistant Pseudomonas aeruginosa[J]. Pept Sci, 2019, 111(1): e23091. DOI:10.1002/bip.23091 |
| [42] |
Yang X, Domalaon R, Lyu YF, et al. Tobramycin-linked efflux pump inhibitor conjugates synergize fluoroquinolones, ri-fampicin and fosfomycin against multidrug-resistant Pseudomonas aeruginosa[J]. J Clin Med, 2018, 7(7): 158. DOI:10.3390/jcm7070158 |
| [43] |
Yang X, Goswami S, Gorityala BK, et al. A tobramycin vector enhances synergy and efficacy of efflux pump inhibitors against multidrug-resistant Gram-negative bacteria[J]. J Med Chem, 2017, 60(9): 3913-3932. DOI:10.1021/acs.jmedchem.7b00156 |
| [44] |
Kamble E, Sanghvi P, Pardesi K. Synergistic effect of antibio-tic combinations on Staphylococcus aureus biofilms and their persister cell populations[J]. Biofilm, 2022, 4: 100068. DOI:10.1016/j.bioflm.2022.100068 |
| [45] |
Chou SL, Shao CX, Wang JJ, et al. Short, multiple-stranded β-hairpin peptides have antimicrobial potency with high selectivity and salt resistance[J]. Acta Biomater, 2016, 30: 78-93. DOI:10.1016/j.actbio.2015.11.002 |
| [46] |
Wang ZY, Zhang LC, Wang J, et al. Synergistic interaction of PMAP-36 and PRW4 with aminoglycoside antibiotics and their antibacterial mechanism[J]. World J Microbiol Biotechnol, 2014, 30(12): 3121-3128. DOI:10.1007/s11274-014-1739-4 |
| [47] |
Domalaon R, Sanchak Y, Koskei LC, et al. Short proline-rich lipopeptide potentiates minocycline and rifampin against multidrug- and extensively drug-resistant Pseudomonas aeruginosa[J]. Antimicrob Agents Chemother, 2018, 62(4): e02374-17. |
| [48] |
Jahangiri A, Neshani A, Mirhosseini SA, et al. Synergistic effect of two antimicrobial peptides, Nisin and P10 with conventional antibiotics against extensively drug-resistant Acinetobacter baumannii and colistin-resistant Pseudomonas aeruginosa isolates[J]. Microb Pathog, 2021, 150: 104700. DOI:10.1016/j.micpath.2020.104700 |
| [49] |
Field D, Seisling N, Cotter PD, et al. Synergistic nisin-polymyxin combinations for the control of Pseudomonas biofilm formation[J]. Front Microbiol, 2016, 7: 1713. |
| [50] |
Lai ZH, Yuan XJ, Chen HY, et al. Strategies employed in the design of antimicrobial peptides with enhanced proteolytic stability[J]. Biotechnol Adv, 2022, 59: 107962. DOI:10.1016/j.biotechadv.2022.107962 |
| [51] |
Almaaytah A, Abualhaijaa A, Alqudah O. The evaluation of the synergistic antimicrobial and antibiofilm activity of AamAP1-Lysine with conventional antibiotics against representative resistant strains of both Gram-positive and Gram-negative bacteria[J]. Infect Drug Resist, 2019, 12: 1371-1380. DOI:10.2147/IDR.S204626 |
| [52] |
Duan HM, Zhang XM, Li Z, et al. Synergistic effect and antibiofilm activity of an antimicrobial peptide with traditional antibiotics against multi-drug resistant bacteria[J]. Microb Pathog, 2021, 158: 105056. DOI:10.1016/j.micpath.2021.105056 |
| [53] |
Memariani H, Memariani M, Shahidi-Dadras M, et al. Melittin: from honeybees to superbugs[J]. Appl Microbiol Biotechnol, 2019, 103(8): 3265-3276. DOI:10.1007/s00253-019-09698-y |
| [54] |
孙楠, 刘又铭, 王倩, 等. 蜂源抗菌肽Melittin与饲料酸化剂协同抑菌效应评价[J]. 饲料研究, 2020, 43(11): 64-67. Sun N, Liu YM, Wang Q, et al. Determination of synergistic antibacterial effect of Melittin and feed acidizing agent acidifier[J]. Feed Research, 2020, 43(11): 64-67. |
| [55] |
Yazici A, Ortucu S, Taskin M, et al. Natural-based antibiofilm and antimicrobial peptides from microorganisms[J]. Curr Top Med Chem, 2018, 18(24): 2102-2107. |
| [56] |
宁亚维, 张明星, 苏丹, 等. 大孔树脂提取侧孢短芽孢杆菌抗菌肽brevilaterin[J]. 食品与发酵工业, 2020, 46(5): 9-16. Ning YW, Zhang MX, Su D, et al. Extraction of antimicro-bial peptide brevilaterin from Brevibacillus laterosporus by macroporous resin[J]. Food and Fermentation Industries, 2020, 46(5): 9-16. DOI:10.13995/j.cnki.11-1802/ts.022612 |
| [57] |
宁亚维, 苏丹, 付浴男, 等. 抗菌肽brevilaterin与柠檬酸联用对大肠杆菌的协同抑菌机理[J]. 食品科学, 2020, 41(19): 31-37. Ning YW, Su D, Fu YN, et al. Antibacterial mechanism of antimicrobial peptide brevilaterin combined with citric acid against Escherichia coli[J]. Food Science, 2020, 41(19): 31-37. |
| [58] |
Li JW, Meng QW, Xing JX, et al. Citric acid enhances clean recycling of Chinese cabbage waste by anaerobic fermentation[J]. J Clean Prod, 2022, 348: 131366. DOI:10.1016/j.jclepro.2022.131366 |
| [59] |
Mirhosseini M, Afzali M. Investigation into the antibacterial behavior of suspensions of magnesium oxide nanoparticles in combination with nisin and heat against Escherichia coli and Staphylococcus aureus in milk[J]. Food Control, 2016, 68: 208-215. DOI:10.1016/j.foodcont.2016.03.048 |
| [60] |
Li QX, Yu SN, Han JZ, et al. Synergistic antibacterial activity and mechanism of action of nisin/carvacrol combination against Staphylococcus aureus and their application in the infecting pasteurized milk[J]. Food Chem, 2022, 380: 132009. DOI:10.1016/j.foodchem.2021.132009 |
| [61] |
Li JJ, Pan D, Yi JJ, et al. Protective effect of β-cyclodextrin on stability of nisin and corresponding interactions involved[J]. Carbohydr Polym, 2019, 223: 115115. DOI:10.1016/j.carbpol.2019.115115 |
| [62] |
van der Does AM, Hiemstra PS, Mookherjee N. Antimicro-bial host defence peptides: immunomodulatory functions and translational prospects[J]. Adv Exp Med Biol, 2019, 1117: 149-171. |
| [63] |
Salouti M, Mirzaei F, Shapouri R, et al. Synergistic antibacterial activity of plant peptide MBP-1 and silver nanoparticles combination on healing of infected wound due to Staphylococcus aureus[J]. Jundishapur J Microbiol, 2016, 9(1): e27997. |
| [64] |
张馨元. 抗菌肽LL-37与酰胺酶联合应用治疗粪肠球菌感染的研究[D]. 呼和浩特: 内蒙古农业大学, 2021. Zhang XY. The effect of the combined use of antimicrobial peptide LL-37 and amidase on Enterococcus faecalis[D]. Hohhot: Inner Mongolia Agricultural University, 2021. |
| [65] |
Han WX, Wei ZQ, Camesano TA. New antimicrobial peptide-antibiotic combination strategy for Pseudomonas aeruginosa inactivation[J]. Biointerphases, 2022, 17(4): 041002. DOI:10.1116/6.0001981 |
| [66] |
Sharma L, Bisht GS. Synergistic effects of short peptides and antibiotics against bacterial and fungal strains[J]. J Pept Sci, 2023, 29(1): e3446. DOI:10.1002/psc.3446 |
| [67] |
Valdez-Miramontes CE, De Haro-Acosta J, Aréchiga-Flores CF, et al. Antimicrobial peptides in domestic animals and their applications in veterinary medicine[J]. Peptides, 2021, 142: 170576. DOI:10.1016/j.peptides.2021.170576 |
| [68] |
王莉, 陈晓, 王书全. 抗菌肽和β-甘露聚糖酶对鹌鹑生长性能及免疫功能的影响[J]. 黑龙江畜牧兽医, 2017(17): 20-23, 26. Wang L, Chen X, Wang SQ. Effects of antimicrobial peptides and β-mannanase on growth performance and immune function of quail[J]. Heilongjiang Animal Science and Veterinary Me-dicine, 2017(17): 20-23, 26. |
| [69] |
刘小龙, 范寰, 陈龙宾, 等. 天蚕素和合生素对AA肉鸡小肠黏膜形态和小肠免疫细胞的影响[J]. 中国畜牧兽医, 2017, 44(11): 3187-3194. Liu XL, Fan H, Chen LB, et al. Effects of cecropin and synbiotics on the intestinal mucosal morphology and intestinal mucosal immune cells of AA broilers[J]. China Animal Husban-dry & Veterinary Medicine, 2017, 44(11): 3187-3194. |
| [70] |
华蕊, 吴科榜, 管庆丰, 等. 猪源抗菌肽PR-39对畜禽常见病原菌的抑菌活性及与抗生素协同杀菌效应研究[J]. 饲料工业, 2019, 40(22): 29-33. Hua R, Wu KB, Guan QF, et al. Antibacterial activity of porcine antibacterial peptide PR-39 against common pathogens in livestock and poultry and its synergistic bactericidal effect with antibiotics[J]. Feed Industry, 2019, 40(22): 29-33. |



