葛根芩连汤源自汉朝张仲景所著《伤寒论》,全方由葛根、黄芩、黄连、炙甘草组成,其中葛根为君药,归脾胃经,养阴生津,解表退热散邪;黄芩、黄连为臣药,入大肠、小肠经,清泄胃肠里热,解毒燥湿;炙甘草甘缓和中,调佐诸药。四药合用,共凑解表清里之功。在辨证论治基础上,现代医学家对葛根芩连汤的临床应用进行了扩展,且疗效显著。为阐明葛根芩连汤的疗效机制,现代学者对其进行了广泛研究。本文从葛根芩连汤的化学物质基础、常用剂型、临床应用、肠道生物学疗效机制等方面进行综述,以期为葛根芩连汤的临床应用和研究提供参考。
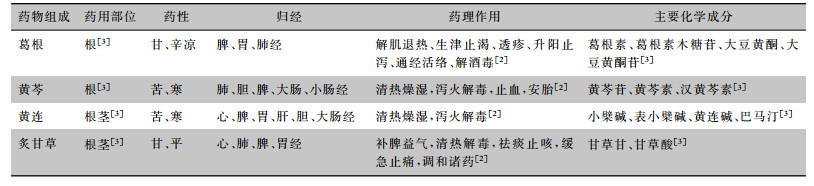
1 葛根芩连汤药物组成、主要化学成分及药理作用葛根芩连汤作为解表清里的经典方剂,配伍精炼,每种药物发挥不同的药效,同时又互相辅佐[1]。方中重用葛根,甘辛而凉,能升阳明清气,亦是治泻良药;黄芩、黄连苦寒清热;炙甘草甘缓和中。四药合用,共奏解表清里之功,兼具抗炎抑菌、抗氧化、降血糖、降血脂等多种药理作用[2]。葛根芩连汤药物组成、主要化学成分及药理作用见表 1。
| 表 1 葛根芩连汤药物组成、主要化学成分及药理作用 |
|
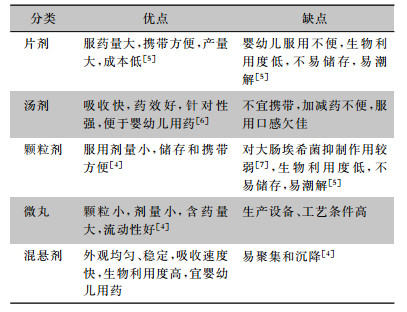
在中医临床治疗疾病时,辨证正确、选方用药恰当是有效治疗疾病的关键,但药物剂型和给药方式直接影响着药效的快慢。随着现代人们生活方式的改变及临床给药方式需求的多样性,需要开发不同剂型以满足各方面要求。目前,已经上市的葛根芩连方常见的剂型有片剂、汤剂、混悬剂、颗粒剂、微丸5种[4],方便个人或临床依据不同需求合理选择。见表 2。
| 表 2 葛根芩连汤常用剂型优缺点比较 |
|
药理研究表明,葛根芩连汤具有清热抗炎、泻火解毒、抗菌、抗氧化、降糖降脂、增强机体免疫等作用[8-10],可用于治疗消化系统疾病、代谢性疾病、心血管系统疾病、上呼吸道感染、神经系统疾病等[11],疗效显著且不良反应少。目前临床主要应用于消化系统疾病,其中以感染性腹泻、肠易激综合征、溃疡性结肠炎、细菌性痢疾、轮状病毒腹泻最为常见。谢伟锋等[12]将左氧氟沙星等喹诺酮类抗菌药物与葛根芩连汤联合使用,治疗感染性腹泻效果更佳,症状消失更快。司徒淳羽[13]发现与双歧杆菌三联活菌等药物相比,葛根芩连汤治疗肠易激综合征的效率更高,不良反应更少。李珊珊[14]采用芍药汤联合葛根芩连汤治疗溃疡性结肠炎,相比于西药,抗炎效果更好,且可避免耐药菌的产生,修护肠道损伤。细菌性痢疾从中医学角度属于湿热痢,临床应用葛根芩连汤加减中药免煎颗粒治疗细菌性痢疾效果较好[15]。将葛根芩连汤联合利巴韦林治疗婴幼儿轮状病毒肠炎伴良性惊厥效果显著,既可抗病毒,还可抗炎,能有效改善症状[16]。可见,葛根芩连汤对肠胃疾病疗效十分显著。
临床上,葛根芩连汤也用于2型糖尿病的治疗。2型糖尿病在中医里属“消渴”范畴,临床常伴有内热症状,如肠道湿热证[17]。马琳娜等[18]在临床采用葛根芩连汤联合二甲双胍治疗2型糖尿病,可有效调节脂代谢水平,取得良好的疗效,且不良反应少。另外,也有关于葛根芩连汤治疗颈动脉粥样硬化、急性化脓性扁桃体炎、肺炎、湿热瘀阻型血管性痴呆、痫病的报道,并取得较好的疗效。可见,广泛挖掘葛根芩连汤对机体的调控机制,并扩大其使用范围,以及未来在临床推广应用是有意义的。
4 葛根芩连汤对肠道屏障的影响口服药物进入胃肠道系统,在肠道中的微生物和酶的作用下被消化、吸收或被转化成有效组分,进一步到达靶点发挥疗效。胃肠道是药物与机体相互作用的第一步,研究药物与胃肠道系统的相互作用,可为药物疗效机制的阐释提供理论基础。葛根芩连汤对多种疾病有效,其治疗机制与其对肠道机械屏障、生物屏障、化学屏障和免疫屏障的调节有关。
4.1 葛根芩连汤对肠道机械屏障的影响肠道是机体与外界直接接触的器官之一。肠道黏膜屏障作为肠道抵抗外界入侵的首要防线,可阻挡外界微生物的侵扰[19]。肠道的机械屏障主要包括上皮细胞和细胞间的紧密连接[20]。每个上皮细胞之间由紧密连接串联在一起[21],作为肠道微生物与免疫系统之间的媒介[22]。当肠道上皮结构异常或细胞间连接被破坏时,肠道的机械屏障受损,肠黏膜通透性增高,进而造成细菌易位使肠道内菌群失调,引发疾病[23]。Occludin、Claudin 1蛋白是构成细胞间紧密连接的重要物质,而细胞间紧密连接是肠道机械屏障最重要的结构。研究[24-25]显示,溃疡性结肠炎小鼠Occludin和Claudin 1蛋白表达下降,肠道黏膜屏障功能损坏,引发炎症反应,葛根芩连汤治疗后,Occludin、Claudin 1蛋白水平升高,炎性因子遭受抑制,肠道黏膜屏障功能得以改善。小肠黏膜的所有上皮细胞来源于隐窝干细胞,隐窝干细胞的发生、分化、增殖、分布等过程直接影响肠黏膜的完整性和功能特异性。仔猪黄痢病因为脾虚湿盛,十二指肠和空肠的结构受到严重损伤,加味葛根芩连汤可促进隐窝干细胞的增殖和分化以维持肠道结构的完整性,降低仔猪空肠的Toll样受体4(TLR4)、肿瘤坏死因子α(TNF-α)、白细胞介素-1β(IL-1β)和白细胞介素-6(IL-6)mRNA水平,进而抑制湿热泄泻仔猪空肠的炎症反应[26]。许琳[27]证实加味葛根芩连汤可下调溃疡性结肠炎小鼠的结肠组织促炎因子IL-1β、IL-6表达水平,诱导E-Cadherin、β-catenin、Occludin、ZO-1表达上调,作用β-catenin/FOSL2/ARID5A通路调控巨噬细胞的极化,进而调节炎症因子的平衡及修护肠黏膜屏障,缓解溃疡性结肠炎症状。
4.2 葛根芩连汤对肠道生物屏障的影响肠道内所含微生物数量巨大,种类繁多,形成了机体重要的生物屏障[28]。人体健康情况下肠道菌群的数量、分布相对平衡稳定,不仅可以减少有害菌对肠道黏膜的损伤,还能参与机体的调控,如促进营养物质消化和吸收[29]。但疾病和其他外界因素会影响肠道菌群数量、活性或导致其移位,造成菌群平衡失调。中药对肠道菌群具有调控作用。苏钢等[30]基于16S高通量测序和网络药理学方法研究了葛根芩连汤治疗抗菌药物相关性腹泻的作用机制,结果显示,葛根芩连汤改善肠道菌群的多样性和结构,尤其是增加乳酸球菌属的丰度,乳酸球菌属可恢复短链脂肪酸中的丁酸盐与丙酸盐的生成,进而抑制NF-κB信号通路中TNF-α、IL-6等炎症因子,激活IL-17信号通路,达到减轻肠道炎症反应、修复肠道黏膜的结果。黄玉龙等[31]发现葛根芩连汤增加腹泻型肠易激综合征肠道的双歧杆菌、嗜酸乳杆菌的数量,调控TNF-α、IL-10等炎症因子的表达。张小兵等[32]研究表明,葛根芩连汤能显著改善湿热型冠心病心绞痛的症状,并提高乳酸杆菌和双歧杆菌的数量,减少肠球菌和大肠埃希菌的数量。对感染性腹泻仔猪模型的研究[33]发现,葛根芩连汤增加细菌的物种丰富度,调节肠道微生物群落的结构,还增加产短链脂肪酸菌的相对丰度,修复肠道黏膜,减轻腹泻。张儒奇等[34]采用葛根芩连汤对腹泻型肠易激综合征大鼠进行干预,通过16S rRNA高通量测序技术检测发现,葛根芩连汤可降低拟杆菌门等致病菌相对丰度并增加厚壁菌门等有益菌相对丰度,改变肠道微生物多样性,影响菌群的结构组成,且拟杆菌门可作用于NF-κB信号通路, 因此减少炎症反应。肠道生物屏障在保护共生细菌生长、促进再生和维持共生稳态以防止微生态失调方面发挥重要作用。葛根芩连汤不仅可调节肠道微生物,还可影响肠道菌群代谢,从而抑制肠道炎症,维持生物屏障内外环境的稳定。
4.3 葛根芩连汤对肠道化学屏障的影响肠上皮细胞分泌的黏液、黏蛋白、消化液、正常菌分泌的抑菌物质及微生物代谢物(短链脂肪酸、胆汁酸、色氨酸等)等共同组成肠道化学屏障。肠道抑菌物质主要有胆汁、黏多糖、溶菌酶和糖蛋白等。黏液层以多种方式将管腔中的细菌与上皮细胞分离。黏液层几小时内更新一次,动态排出细菌并限制其进入上皮[35]。黏蛋白主要由杯状细胞分泌,为黏液层提供结构框架。黏液层可能含有30种核心蛋白,如黏蛋白、抗菌肽和分泌型免疫球蛋白A(IgA)等,其中结肠表面的杯状细胞持续分泌Muc2来维持黏液层的完整性[36]。方剂对肠道微生物进行调节的同时也调控肠道代谢。短链脂肪酸的组成主要由菌群结构决定,能抑制肠道有害菌生长、调节肠道pH值[37];胆汁酸主要促进脂质及脂溶性维生素在体内溶解、消化和吸收[38];色氨酸是人体必需氨基酸之一,可以激活芳香烃受体(aryl hydrocarbon receptor, AhR)信号通路,降低肠道炎症[39]。尽管肠道微生物代谢物作用有所不同,但最终都是抑制炎症和促进紧密连接蛋白以及黏蛋白表达来保护肠道屏障[29]。Wang等[40]发现葛根芩连汤通过调节溃疡性结肠炎小鼠肠道微生物的色氨酸代谢来激活AhR,且增加了肠上皮黏蛋白的水平,并恢复上皮细胞紧密连接的完整性,来修复肠道屏障的结构,降低肠道屏障的通透性。Muc4可参与免疫反应,而Muc13对结肠上皮细胞有保护作用。致肠毒素大肠埃希菌(enterotoxin Escherichia coli, ETEC)会引起断奶后仔猪严重腹泻,Liu等[41]在研究葛根芩连汤中葛根素、黄芩素和盐酸小檗碱对ETEC感染猪肠上皮细胞的调控作用时发现,葛根素可显著降低Muc13 mRNA的水平,黄芩苷可显著降低Muc4和Muc13 mRNA的水平,盐酸小檗碱减少了肠上皮细胞表面的细菌数量。
4.4 葛根芩连汤对肠道免疫屏障的影响肠道不但是人体最大的消化器官,还是机体最大的免疫器官[42]。肠道免疫屏障主要包括免疫细胞(巨噬细胞、DC细胞、T细胞、B细胞)和相关淋巴细胞组织。巨噬细胞是肠道微环境稳态的关键调节因子,有促炎和抗炎两种功能,在肠道慢性炎症的调控及肠上皮的损伤后修复中发挥关键作用。加味葛根芩连汤可下调溃疡性结肠炎小鼠M1巨噬细胞而升高M2巨噬细胞比例数量,调控巨噬细胞的极化,修护肠黏膜完整性,改善结肠炎的症状[27]。对溃疡性结肠炎的研究[43]发现,葛根芩连汤对MPO活性和IL-1β、TNF-α、IL-6、转化生长因子-β1(TGF-β1)及白细胞介素-17(IL-17)炎症因子的表达具有抑制作用,并且双向调节Notch信号来维持黏膜稳态。Notch信号在急性溃疡性结肠炎小鼠中活跃,而在慢性溃疡性结肠炎小鼠中不活跃。葛根芩连汤在急性溃疡性结肠炎模型中下调Hes1、RBP-J和MAML蛋白并增强杯状细胞,而在慢性溃疡性结肠炎小鼠中上调Hes1、RBP-J和MAML蛋白,减少杯状细胞分化并促进隐窝基底柱状(CBC)干细胞增殖[44]。此外,通过降低黏膜中TLR4的表达和NF-κB的激活,并伴随着结肠中几种炎症细胞因子(TNF-α、IL-6、IL-1β和IL-4)的下调,增强抗氧化作用,也是葛根芩连汤治疗溃疡性结肠炎的作用机制[45]。Luo等[46]研究表明葛根芩连汤能通过促进乳酸菌生长和抑制TLR2/ MyD88/NF-κB信号通路治疗感染性腹泻,恢复肠黏膜屏障。Ma等[47]研究证实,加味葛根芩连汤在治疗溃疡性结肠炎时,抑制NLRP3炎症小体相关信号通路的激活,减少γδT17细胞的激活,从而调节免疫炎症反应,修护肠道黏液屏障。目前,炎症信号通路的研究较多,这些结果揭示葛根芩连汤抗炎作用的机制,同时也提示,方剂通过调控肠道免疫功能发挥其肠道保护作用。
5 结论及展望中医药是中华民族的瑰宝,是5 000多年文明的结晶,在疾病预防、治疗、康复方面具有独特的优势。深入挖掘中医药资源,阐释其疗效的科学原理,对推动中医药的发展和临床应用具有重要意义。葛根芩连汤是解表清里的经典方剂,在现代临床有着广泛应用。现代学者对葛根芩连汤的临床应用投入了大量研究,揭示葛根芩连汤可修复肠道屏障。然而,中药疗效的发挥是多靶点的,对葛根芩连汤的作用机制研究还需深入。虽然目前对葛根芩连汤的研究有一定的成果,但对于很多基础性疾病,单用葛根芩连汤只能缓解和改善,对如何提高疗效仍有较大探索空间。基于此,以下几点仍需思考:①目前临床上更多使用葛根芩连汤与其他药联用或者配伍其他中药成分,发挥更好的互补和协同作用,增大临床疗效,扩宽应用范围。②药物剂型在发挥药效时也是很重要的因素,可从药物剂型和剂型材料着手,借鉴新技术、新方法、新理念,寻找更高效、更安全的剂型材料和剂型。③关于葛根芩连汤对肠道屏障的影响,如今大量研究都是关于肠胃疾病,而葛根芩连汤治疗其他疾病时对肠道屏障和肠道微生态机制的研究较少,此部分有待深入认识。葛根芩连汤在治疗各科疾病中都能取得良好的疗效,发展前景广泛,因此应该更深入地探究,以期为临床应用提供参考,促进中药未来发展。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Xu XZ, Gao ZZ, Yang FQ, et al. Antidiabetic effects of Gegen Qinlian Decoction via the gut microbiota are attributable to its key ingredient berberine[J]. Genomics Proteomics Bioinformatics, 2020, 18(6): 721-736. DOI:10.1016/j.gpb.2019.09.007 |
| [2] |
钟赣生, 杨柏灿. 中药学[M]. 5版. 北京: 中国中医药出版社, 2021. Zhong GS, Yang BC. Chinese pharmacy[M]. 5th ed. Beijing: China Press of Traditional Chinese Medicine, 2021. |
| [3] |
国家药典委员会. 中华人民共和国药典-一部[M]. 北京: 中国医药科技出版社, 2015. National Pharmacopoeia Commission. Pharmacopoeia of the China-volume Ⅰ[M]. Beijing: China Medical Science and Technology Press, 2015. |
| [4] |
张明明. 葛根芩连混悬剂制备工艺研究[D]. 广州: 南方医科大学, 2012. Zhang MM. Study on preparation technology for Gegenqinlian suspension[D]. Guangzhou: Southern Medical University, 2012. |
| [5] |
曹越, 姚完美, 刘昕, 等. 探讨泻心汤类方群及其复方制剂剂型研究[J]. 辽宁中医药大学学报, 2023, 25(7): 148-155. Cao Y, Yao WM, Liu X, et al. Study on Xiexin Decoction and its compound preparation[J]. Journal of Liaoning University of Traditional Chinese Medicine, 2023, 25(7): 148-155. DOI:10.13194/j.issn.1673-842x.2023.07.031 |
| [6] |
刘莲萱, 吴威, 庞琳琳, 等. 葛根芩连汤化学成分、药理作用及临床应用研究进展[J]. 中华中医药学刊, 2022, 40(3): 147-154. Liu LX, Wu W, Pang LL, et al. Research progress on chemical composition, pharmacological action and clinical application of Gegen Qinlian Decoction[J]. Chinese Archives of Traditio-nal Chinese Medicine, 2022, 40(3): 147-154. DOI:10.13193/j.issn.1673-7717.2022.03.034 |
| [7] |
陈丽红, 唐于平, 王强. 葛根芩连煎剂与颗粒剂的抗腹泻、抑菌药效研究[J]. 中国药房, 2012, 23(39): 3649-3651. Chen LH, Tang YP, Wang Q. Study on anti-diarrhea and antibacterial efficacy of Gegen Qinlian Decoction and granule[J]. China Pharmacy, 2012, 23(39): 3649-3651. DOI:10.6039/j.issn.1001-0408.2012.39.01 |
| [8] |
熊淑平, 章常华, 邓永兵, 等. 葛根芩连汤改善KK-Ay糖尿病小鼠糖脂代谢作用的实验研究[J]. 时珍国医国药, 2016, 27(9): 2090-2092. Xiong SP, Zhang CH, Deng YB, et al. Effects of Gegen Qinlian Decoction on glucose and lipid metabolism in KK-Ay diabetic mice[J]. Lishizhen Medicine and Materia Medica Research, 2016, 27(9): 2090-2092. |
| [9] |
续畅, 钟萌, 马致洁, 等. 葛根芩连汤的现代研究进展[J]. 吉林中医药, 2015, 35(6): 629-632. Xu C, Zhong M, Ma ZJ, et al. Research status of Gegen Qinlian decoction[J]. Jilin Journal of Traditional Chinese Medicine, 2015, 35(6): 629-632. DOI:10.13463/j.cnki.jlzyy.2015.06.031 |
| [10] |
姜璎娜, 曾治君, 傅灵艳, 等. 基于肠道菌群研究葛根芩连汤降脂并预防血糖升高的作用机制[J]. 中国药房, 2020, 31(15): 1823-1829. Jiang YN, Zeng ZJ, Fu LY, et al. Study on the mechanism of Gegen Qinlian Decoction for lowering blood lipids and preventing blood glucose increase based on intestinal flora[J]. China Pharmacy, 2020, 31(15): 1823-1829. DOI:10.6039/j.issn.1001-0408.2020.15.06 |
| [11] |
黄鑫磊, 贾雪雯, 丁元庆. 葛根芩连汤临床应用进展[J]. 山东中医药大学学报, 2020, 44(2): 215-220. Huang XL, Jia XW, Ding YQ. Review on clinical application of Gegen Qinlian Decoction[J]. Journal of Shandong University of Traditional Chinese Medicine, 2020, 44(2): 215-220. DOI:10.16294/j.cnki.1007-659x.2020.02.020 |
| [12] |
谢伟锋, 王祖棣. 葛根芩连汤联合左氧氟沙星治疗湿热下注型感染性腹泻的效果分析[J]. 北方药学, 2021, 18(5): 30-31. Xie WF, Wang ZD. Effect of Gegen Qinlian Decoction combined with levofloxacin in the treatment of infectious diarrhea with damp-heat downward injection[J]. Journal of North Pharmacy, 2021, 18(5): 30-31. DOI:10.3969/j.issn.1672-8351.2021.05.014 |
| [13] |
司徒淳羽. 葛根芩连汤治疗脾胃湿热型腹泻型肠易激综合征的临床效果[J]. 内蒙古中医药, 2022, 41(2): 65-66. Situ CY. Clinical effect of Gegen Qinlian Decoction in the treatment of diarrhea-predominant irritable bowel syndrome with spleen-stomach damp-heat type[J]. Inner Mongolia Journal of Traditional Chinese Medicine, 2022, 41(2): 65-66. |
| [14] |
李姗姗. 芍药汤合葛根芩连汤治疗溃疡性结肠炎的效果观察[J]. 中国社区医师, 2023, 39(2): 93-95. Li SS. Effect observation of Shaoyao Decoction and Gegen Qinlian Decoction in treatment of ulcerative colitis[J]. Chinese Community Doctors, 2023, 39(2): 93-95. |
| [15] |
赵学顺, 彭桂华. 葛根芩连汤加减中药免煎颗粒与传统饮片治疗细菌性痢疾的对照观察实践思考[J]. 临床医药文献电子杂志, 2017, 4(70): 13790. Zhao XS, Peng GH. Comparison of Gegen Qinlian Decoction and traditional Chinese medicine non-decoction granules in the treatment of bacillary dysentery[J]. Electronic Journal of Clinical Medical Literature, 2017, 4(70): 13790. DOI:10.3877/j.issn.2095-8242.2017.70.113 |
| [16] |
朱勃, 孙媛. 葛根芩连汤联合利巴韦林治疗婴幼儿轮状病毒肠炎伴良性惊厥的临床效果[J]. 临床医学研究与实践, 2022, 7(8): 125-128. Zhu B, Sun Y. Clinical effect of Gegen Qinlian Decoction combined with ribavirin in the treatment of infantile rotavirus enteritis complicated with benign convulsion[J]. Clinical Research and Practice, 2022, 7(8): 125-128. |
| [17] |
王艳, 梁建庆, 朱向东, 等. 清热类复方改善2型糖尿病的作用机制研究进展[J]. 中国中药杂志, 2023, 48(7): 1711-1723. Wang Y, Liang JQ, Zhu XD, et al. Mechanism of heat-clea-ring prescriptions in alleviating type 2 diabetes mellitus: a review[J]. China Journal of Chinese Materia Medica, 2023, 48(7): 1711-1723. |
| [18] |
马琳娜, 薛毅, 王韧舟. 葛根芩连汤联合二甲双胍治疗2型糖尿病患者的疗效观察[J]. 世界中西医结合杂志, 2022, 17(10): 2092-2095. Ma LN, Xue Y, Wang RZ. Clinical efficacy of Gegen Qinlian Decoction combined with metformin in treatment of type 2 diabetes mellitus[J]. World Journal of Integrated Traditional and Western Medicine, 2022, 17(10): 2092-2095. |
| [19] |
Wang K, Wu LY, Dou CZ, et al. Research advance in intestinal mucosal barrier and pathogenesis of Crohn's disease[J]. Gastroenterol Res Pract, 2016, 2016: 9686238. |
| [20] |
舒雁, 惠华英, 谭周进. 肠道短链脂肪酸与腹泻的相关性研究进展[J]. 中国感染控制杂志, 2022, 21(9): 937-943. Shu Y, Hui HY, Tan ZJ. Advances in correlation between short-chain fatty acids and diarrhea[J]. Chinese Journal of Infection Control, 2022, 21(9): 937-943. |
| [21] |
Chelakkot C, Ghim J, Ryu SH. Mechanisms regulating intestinal barrier integrity and its pathological implications[J]. Exp Mol Med, 2018, 50(8): 1-9. |
| [22] |
Peterson LW, Artis D. Intestinal epithelial cells: regulators of barrier function and immune homeostasis[J]. Nat Rev Immunol, 2014, 14(3): 141-153. |
| [23] |
惠华英, 何云山, 吴仪, 等. 肠道湿热证泄泻小鼠模型的研制及葛根芩连汤疗效[J]. 中国中医基础医学杂志, 2021, 27(9): 1380-1385. Hui HY, He YS, Wu Y, et al. Establishment of a diarrheal mouse model with intestinal dampness-heat syndrome and the effects of Gegen Qinlian Decoction[J]. Journal of Basic Chinese Medicine, 2021, 27(9): 1380-1385. |
| [24] |
谭悦, 郑长清. 紧密连接蛋白occludin、ZO-1在溃疡性结肠炎中的表达及其临床意义[J]. 现代药物与临床, 2018, 33(7): 1803-1808. Tan Y, Zheng CQ. Expression and clinical significance of tight junction protein occludin and ZO-1 in ulcerative colitis[J]. Drugs & Clinic, 2018, 33(7): 1803-1808. |
| [25] |
郑晨曦, 冯嘉轩, 陈昭彤, 等. 葛根芩连汤对溃疡性结肠炎小鼠肠道屏障的保护作用机制[J]. 中国兽医学报, 2023, 43(3): 571-576. Zheng CX, Feng JX, Chen ZT, et al. Protective mechanism of Gegen Qinlian Decoction on intestinal barrier in mice with ulcerative colitis[J]. Chinese Journal of Veterinary Science, 2023, 43(3): 571-576. |
| [26] |
刘晓曦. 加味葛根芩连汤对湿热泄泻仔猪肠道和体外肠上皮细胞损伤的调控机理[D]. 北京: 中国农业大学, 2017. Liu XX. The mechanism of Gegen Qinlian Decoction regulating the intestinal damage in piglets and the intestinal epithelial cells in vitro caused by Shi-Re-Xie-Xie[D]. Beijing: China Agricultural University, 2017. |
| [27] |
许琳. 基于β-catenin/FOSL2/ARID5A通路探讨加味葛根芩连汤调控UC巨噬细胞极化的作用机制[D]. 北京: 中国中医科学院, 2021. Xu L. Based on β-catenin/FOSL2/ARID5A pathway to explore the mechanism of modified Gegen Qinlian Decoction on regulating macrophages polarization in ulcerative colitis[D]. Beijing: China Academy of Chinese Medical Sciences, 2021. |
| [28] |
Lavelle A, Sokol H. Gut microbiota-derived metabolites as key actors in inflammatory bowel disease[J]. Nat Rev Gastro- enterol Hepatol, 2020, 17(4): 223-237. |
| [29] |
张德明, 黄嘉訸, 李劲树, 等. 猪肠道微生物及其代谢产物与肠道屏障研究进展[J]. 畜牧兽医学报, 2022, 53(5): 1334-1344. Zhang DM, Huang JH, Li JS, et al. Research progress of gut microbiota, metabolites and gut barrier in pigs[J]. Acta Vete-rinaria et Zootechnica Sinica, 2022, 53(5): 1334-1344. |
| [30] |
苏钢, 杨光勇, 张庚鑫, 等. 基于16S rRNA测序与网络药理学探讨葛根芩连汤干预抗生素相关性腹泻的作用机制[J]. 中国实验方剂学杂志, 2023, 29(23): 81-88. Su G, Yang GY, Zhang GX, et al. Study on the mechanism of Gegen Qinlian Decoction in the intervention of antibiotic-associated diarrhea based on 16S rRNA sequencing and network pharmacology[J]. Chinese Journal of Experimental Traditional Medical Formulae, 2023, 29(23): 81-88. |
| [31] |
黄玉龙, 李枝锦, 吴平财. 葛根芩连汤治疗腹泻型肠易激综合征脾胃湿热证疗效观察与机制研究[J]. 中国中医基础医学杂志, 2022, 28(12): 2015-2017. Huang YL, Li ZJ, Wu PC. Effect and mechanism of Gegen Qinlian Decoction in the treatment of diarrhea-predominant irritable bowel syndrome with spleen-stomach damp-heat syndrome[J]. Journal of Basic Chinese Medicine, 2022, 28(12): 2015-2017. |
| [32] |
张小兵, 曾玲玲, 刘云, 等. 葛根芩连汤治疗湿热型冠心病心绞痛的疗效及对肠道菌群的影响[J]. 中国临床研究, 2022, 35(12): 1737-1740. Zhang XB, Zeng LL, Liu Y, et al. Curative effect of Gegen Qinlian Decoction on damp-heat type coronary heart disease with angina pectoris and its influence on intestinal flora[J]. Chinese Journal of Clinical Research, 2022, 35(12): 1737-1740. |
| [33] |
Liu CS, Liang X, Wei XH, et al. Gegen Qinlian Decoction treats diarrhea in piglets by modulating gut microbiota and short-chain fatty acids[J]. Front Microbiol, 2019, 10: 825. |
| [34] |
张儒奇, 方志安, 韩文庆, 等. 葛根芩连汤对腹泻型肠易激综合征大鼠肠道菌群的影响[J]. 中国中药杂志, 2022, 47(24): 6709-6719. Zhang RQ, Fang ZA, Han WQ, et al. Effect of Gegen Qinlian Decoction on gut microbiota of irritable bowel syndrome with diarrhea rats[J]. China Journal of Chinese Materia Medica, 2022, 47(24): 6709-6719. |
| [35] |
Capaldo CT, Powell DN, Kalman D. Layered defense: how mucus and tight junctions seal the intestinal barrier[J]. J Mol Med, 2017, 95(9): 927-934. |
| [36] |
Johansson MEV. Fast renewal of the distal colonic mucus la-yers by the surface goblet cells as measured by in vivo labeling of mucin glycoproteins[J]. PLoS One, 2012, 7(7): e41009. |
| [37] |
Joshi A, Guo JX, Holleran JL, et al. Evaluation of the pharmacokinetic drug-drug interaction potential of iohexol, a renal filtration marker[J]. Cancer Chemother Pharmacol, 2020, 86(4): 535-545. |
| [38] |
孔祎頔, 李民, 王桂芹. 动物胆汁酸代谢与肠道微生态的互作关系[J]. 中国畜牧杂志, 2020, 56(8): 38-44. Kong YD, Li M, Wang GQ. Interaction between bile acid metabolism and intestinal micro-ecology in animals[J]. Chinese Journal of Animal Science, 2020, 56(8): 38-44. |
| [39] |
Liang HW, Dai ZL, Kou J, et al. Dietary l-tryptophan supplementation enhances the intestinal mucosal barrier function in weaned piglets: implication of tryptophan-metabolizing microbiota[J]. Int J Mol Sci, 2019, 20(1): 20. |
| [40] |
Wang XJ, Huang SW, Zhang ML, et al. Gegen Qinlian Decoction activates AhR/IL-22 to repair intestinal barrier by modulating gut microbiota-related tryptophan metabolism in ulcerative colitis mice[J]. J Ethnopharmacol, 2023, 302(Pt B): 115919. |
| [41] |
Liu XX, Liu FH, Ma YF, et al. Effect of puerarin, baicalin and berberine hydrochloride on the regulation of IPEC-J2 cells infected with enterotoxigenic Escherichia coli[J]. Evid Based Complement Alternat Med, 2019, 2019: 7438593. |
| [42] |
Bain CC, Scott CL, Uronen-Hansson H, et al. Resident and pro-inflammatory macrophages in the colon represent alternative context-dependent fates of the same Ly6Chi monocyte precursors[J]. Mucosal Immunol, 2013, 6(3): 498-510. |
| [43] |
Zhao YX, Luan HF, Jiang H, et al. Gegen Qinlian Decoction relieved DSS-induced ulcerative colitis in mice by modulating Th17/Treg cell homeostasis via suppressing IL-6/JAK2/STAT3 signaling[J]. Phytomedicine, 2021, 84: 153519. |
| [44] |
Zhao YX, Luan HF, Gao H, et al. Gegen Qinlian Decoction maintains colonic mucosal homeostasis in acute/chronic ulcerative colitis via bidirectionally modulating dysregulated Notch signaling[J]. Phytomedicine, 2020, 68: 153182. |
| [45] |
Li RY, Chen YY, Shi MJ, et al. Gegen Qinlian Decoction alleviates experimental colitis via suppressing TLR4/NF-κB signaling and enhancing antioxidant effect[J]. Phytomedicine, 2016, 23(10): 1012-1020. |
| [46] |
Luo ZY, Liu CS, Hu YN, et al. Gegen Qinlian Decoction restores the intestinal barrier in bacterial diarrhea piglets by promoting Lactobacillus growth and inhibiting the TLR2/MYD88/NF-κB pathway[J]. Biomed Pharmacother, 2022, 155: 113719. |
| [47] |
Ma J, Zhang JQ, Wang YF, et al. Modified Gegen Qinlian Decoction ameliorates DSS-induced chronic colitis in mice by restoring the intestinal mucus barrier and inhibiting the activation of γδT17 cells[J]. Phytomedicine, 2023, 111: 154660. |



