随着抗菌药物的广泛应用,病原菌的多重耐药性成为公共卫生面临的一个严峻挑战,2019年抗菌药物耐药性被世界卫生组织(WHO)列为全球健康十大威胁之一[1]。日益突出的多重耐药菌(multidrug-resistant organism, MDRO)感染严重威胁医疗质量与患者安全,导致沉重的疾病负担[2]。我国高度重视微生物耐药防控工作,2021年实施的《中华人民共和国生物安全法》[3],将应对微生物耐药上升至国家战略高度。重症监护病房(ICU)患者由于菌群改变、免疫反应受损、侵入性操作破坏解剖完整性,是MDRO感染发生率最高的人群之一[4-5]。目前MDRO感染防控措施主要包括医务人员手卫生、环境物体表面清洁消毒、接触隔离等综合防控措施[6],且由于主动筛查较高的成本-效益比,大部分医院ICU未实行MDRO主动筛查[7-8]。近年来,在基于数据推进临床决策的背景下,通过建立风险预测模型,实现早期识别、监测和预警,已成为ICU MDRO感染防控研究领域的热点。国内外构建了多个ICU MDRO感染相关预测模型,但现有模型的预测性能和临床适用性仍待进一步验证。本研究旨在梳理和总结现有ICU MDRO感染风险预测模型研究,评价偏倚风险与适用性,以期为后续模型建立及应用提供参考依据。
1 资料与方法 1.1 纳入与排除标准纳入标准:①研究对象为ICU患者;②研究内容为MDRO感染风险预测模型的构建。排除标准:①模型在特定人群中建立,如肝移植术后或仅包含男性/女性/儿童/老年人;②未描述模型构建过程或方法;③不能获取原文或数据不完整;④非原始研究。
1.2 文献检索策略计算机检索PubMed、Embase、Web of Science、Cochrane Library、CINAHL、CBM、万方和中国知网等数据库,检索时限均为建库至2022年6月1日。英文检索词为:drug resis-tance, multiple, bacterial, multiple antibacterial drug resistance, multidrug-resistant organisms, intensive care units, ICU, prediction model, risk prediction, risk score, risk assessment等。中文检索词为:多重耐药菌、ICU、重症监护病房、预测、模型、风险评分等。检索策略以主题词结合自由词,并辅以文献追溯等方法。以PubMed为例,其具体检索策略如下:(“drug resistance, multiple, bacterial”[MeSH Terms] OR “multiple antibacterial drug resistance”[Title/Abstract] OR “multi drug-resistant organisms”[Title/Abstract] OR “drug resistance multiple”[Title/Abstract] OR “multi drug-resistant bacteria”[Title/Abstract]) AND (“INTENSIVE CARE UNITS”[MeSH Terms] OR “intensive care unit”[Title/Abstract] OR “unit intensive care”[Title/Abstract] OR “ICU”[Title/Abstract]) AND (“prediction model”[Title/Abstract] OR “risk prediction”[Title/Abstract] OR “model”[Title/Abstract] OR “risk score”[Title/Abstract] OR “risk assessment”[Title/Abstract])。
1.3 文献筛选及资料提取方法由2名研究者独立筛选文献、提取资料并交叉核对。导入EndNote20去重后,阅读文题、摘要初筛,再阅读全文进行二次筛选,遇分歧时与第三方讨论解决。根据预测模型构建研究数据提取和质量评价清单(Checklist for Critical Appraisal and Data Extraction for Systematic Reviews of Prediction Modelling Stu-dies,CHARMS)[9]进行信息提取,提取内容包括:①研究基本信息,包括年份、国家、研究对象、设计类型、预测结局;②模型建立情况及预测性能,包括变量处理及筛选方法、样本量、缺失数据、模型建立及验证方法、模型性能等;③模型呈现形式。
1.4 文献质量评价方法由2名研究者采用风险预测模型评估工具(Prediction Model Risk of Bias Assessment Tool, PROBAST)[10-11]对纳入文献偏倚风险、适用性独立进行评价,遇分歧时与第三方讨论解决。
2 结果 2.1 文献筛选流程及结果初步检索文献共838篇,经过浏览文献题目和摘要,排除重复文献及标题、主题不符文献,最终纳入17篇文献[12-28]。文献筛选流程和结果见图 1。
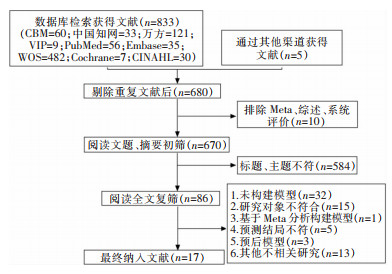 |
| 图 1 文献筛选流程图 Figure 1 Flow chart of literature screening |
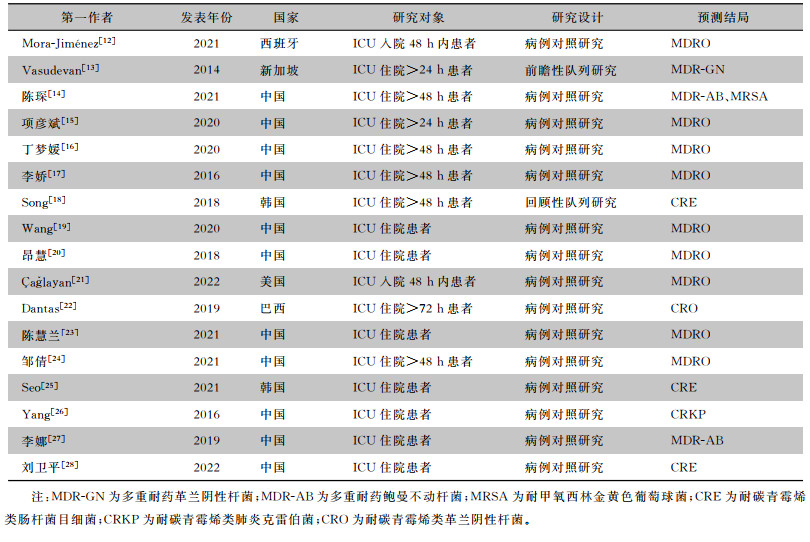
纳入研究基本特征见表 1。
| 表 1 纳入研究基本特征 Table 1 General characteristics of included studies |
|
各研究样本总量为82~4 503例,结果事件数与协变量个数比(the number of events per variable,EPV)在5.17~264.00。11项研究[13-18, 20-21, 23-24, 28]将连续变量转换为分类变量。在预测变量的选择上,8项研究[13, 16-20, 22, 25]使用逐步回归,包括向前、向后、逐步选择;7项研究[14-15, 23-24, 26-28]仅通过单因素分析筛选变量;Song等[18]考虑到交互变量的筛选,联合运用决策树分析和向前逐步回归;Çaǧlayan等[21]运用最小绝对收缩和选择算法(least absolute shrinkage and selection operator, LASSO)筛选变量。纳入模型应用了多种建模方法,13项研究[13, 15-20, 22-23, 25-28]采用逻辑回归(logistic regression, LR),3项研究[12, 14, 21]采用机器学习(machine learning,ML),包括决策树(decision tree, DT)、人工神经网络(artificial neural network, ANN)、随机森林(random forest, RF)、极端梯度提升算法(eX-treme gradient boosting, XGB),1项研究[24]运用判别分析。在缺失数据方面,1项研究[19]报告了缺失例数并采用蒙特卡洛多重插补处理。模型中纳入的预测因子主要分为5类:人口社会学特征、医疗情况、诊断及检验结果、药物使用情况、侵入性操作。各模型出现最多的预测因子:抗菌药物使用(n=10)、机械通气(n=9)、ICU住院时间(n=8)、留置导尿管(n=7)、性别(n=4)、基础疾病(n=3)、共病(n=3)。模型建立情况及预测性能见表 2。
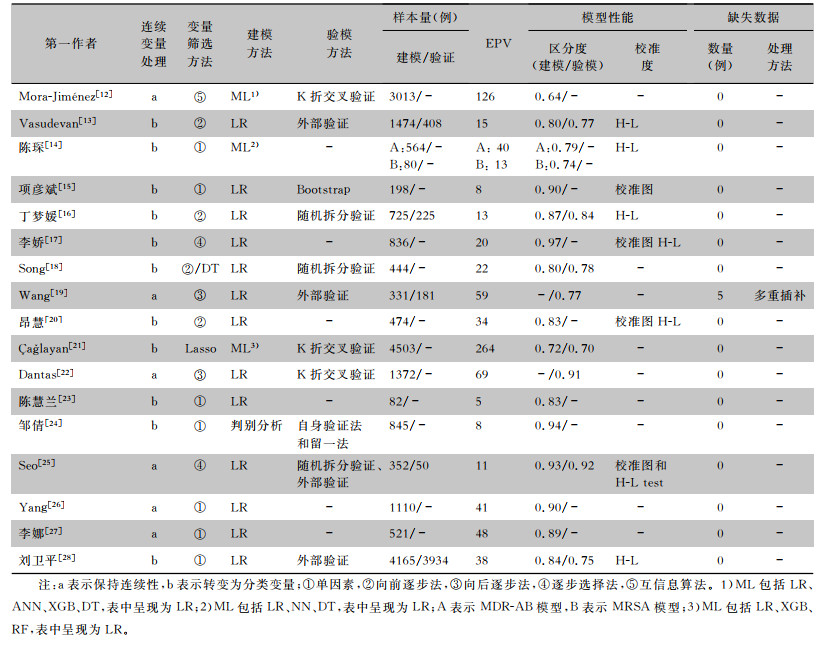
| 表 2 ICU MDRO感染风险预测模型建立情况及预测性能 Table 2 Establishment and performance of the prediction models for MDRO infection in ICU |
|
模型预测性能主要包括区分度和校准度,区分度是指模型区分是否发生预期事件的能力,主要通过受试者工作特征曲线下面积(area under the curve,AUC)表示;校准度是反映模型预测结果与实际结果一致性的综合指标,通过Hosmer-Lemeshow拟合优度检验(H-L检验)和绘制校准图进行综合评价[10]。有9项研究[12, 18-19, 21-24, 26-27]仅报告了区分度指标,而未报告校准度指标。纳入模型具有良好区分度(AUC为0.64~0.94),除Mora-Jiménez等[12]的研究外,其余模型AUC均>0.7。8项研究报告了校准度,其中4个模型[15, 17, 20, 25]中正确使用校准图进行了评价,其余4项研究仅报告了H-L拟合优度检验。1个研究[19]报告了临床决策曲线。在模型验证集选择方面,7项研究基于模型开发队列数据进行了内部验证,包括K折交叉验证[12, 21-22]、留一法[18]、计算机模拟重复采样法(Bootstrap)[15]、随机拆分验证[16, 25]。有4项研究[13, 19, 25, 28]利用同一中心不同时间段的研究对象进行了外部验证。见表 2。
2.5 模型呈现形式纳入模型包含的预测因子3~24个,14个模型报告了最终模型的呈现,见表 3。3项研究[15, 19, 25]运用列线图,3项研究[13, 16, 28]以加和评分的形式呈现,并且进行了风险值分层,Çaǧlayan等[18]将模型制作为网页计算器,其余7项研究[14, 17-18, 20, 23-24, 27]均以回归方程形式呈现。具体的模型呈现见表 3。
| 表 3 ICU MDRO感染风险预测模型的模型报告 Table 3 Model reports of MDRO infection prediction models in ICU |

|
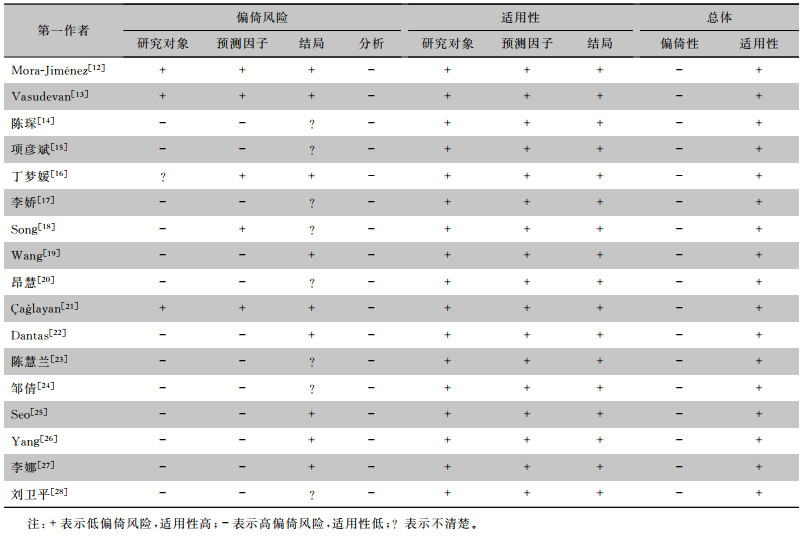
17个模型中,分别有3(17.65%)、5(29.41%)、9(52.94%)和0个模型在研究对象、预测因子、结局和统计分析领域被评为低风险,见表 4。前3个领域的主要问题分别为:研究设计不恰当(采用病例对照研究,n=5,88.24%),纳入与排除标准不恰当(排除资料不完善、数据缺失患者以及未报告纳入与排除标准,导致选择性偏倚风险增加,n=2,11.76%);未报告盲法的使用情况(n=11,64.70%)。统计分析领域问题较严重,主要集中在样本量不足,即EPV<20(n=7,41.18%)、内部验证使用不当(未进行内部验证或仅包含随机拆分验证法,n=8,47.06%)、连续变量处理不恰当(将连续变量转换为分类变量,n=10,58.82%)、缺失数据处理不当(n=2,11.76%)和模型表现评价不完整(仅报告了区分度指标,而未报告校准度指标,n=8,47.06%;研究中没有校准图或表格,仅报告校准的统计数据或仅使用H-L检验,n=3,17.65%),仅运用单因素分析筛选预测因子(n=5,29.41%)。
| 表 4 纳入模型的偏倚风险及适用性评价结果 Table 4 Evaluations of the bias risk and applicability of the included models |
|
纳入模型整体适用性较好,见表 4,因为易于临床上找到应用对象,且参考了与临床诊断、检验、治疗相关的变量,因此在临床实践中易得到应用。
3 讨论本研究中纳入的预测模型来自中国、韩国、新加坡、美国、西班牙、巴西,不同人群间MDRO感染发病率、风险因素水平分布等存在差异,模型结果也不同。超过半数在亚洲开展,一项全球调查显示ICU患者感染比率最高的是亚洲[29],达到了60%。在预测因子差异方面,最常见的预测因子是抗菌药物,西班牙[12]、韩国[18, 25]、新加坡[13]更关注特定抗菌药物种类的用药史如头孢菌素类、碳青霉烯类,而中国除了抗菌药物种类也关注其联用情况[14, 20]、使用时间[14, 24, 26]。此外,只有中国的4个预测模型[16, 19, 24, 26]将性别作为预测因子,可能原因是男性相对于女性更有可能发生多发伤,从而导致MDRO感染的发生[30]。共病作为常见预测因子之一,不同人群中也存在差异,如西班牙[12]和巴西[22]分别是肿瘤、COPD共病。中国[24]的模型区分度最好,西班牙[12]的相对最差,由于目前国内外研究均未将模型作用于外部临床实践,无法进一步比较性能。
碳青霉烯类抗生素作为临床抗感染治疗的药物,从20世纪80年代首次引入,至今仍发挥着关键作用[31],碳青霉烯类耐药菌的产生导致临床感染控制面临严峻挑战,因此现有研究较关注耐碳青霉烯类细菌感染的预测[18, 22, 26, 28]。考虑到不同等级医院在分离菌株种类、比例、耐药性及医疗资源分布上也存在差别,Seo等[25]基于韩国的二级医院构建了CRE感染风险预测模型,以减少不同等级医院感染防控差距,纳入了APACHE Ⅱ、中心静脉置管、鼻胃管、使用头孢菌素类抗生素4个预测因子。此外,随着研究者将防控关口前移[12, 21],即对ICU新入住患者MDRO定植或感染进行预测,入院时即可快速识别感染或无症状定植患者,减少确定患者感染状态的“滞后”影响(病原菌培养及药敏试验时间24~72 h)[32]。从而实施MDRO定植、感染不同阶段的防控策略以降低病原菌传播和后续感染,实现早发现、早隔离、早防控。构建ICU MDRO感染风险预测模型,需结合地区流行病学、明确防控关口及不同等级医院菌株情况与资源分布,以增大模型的临床推广应用价值。
纳入模型中16个模型AUC>0.7,灵敏度、特异度分别为25.0%~99.2%、66.5%~98.0%。模型预测性能较好,但模型开发和验证中存在一些方法学缺陷,导致纳入研究偏倚风险普遍较高,未来相关模型研究过程中应重视并进一步完善。在研究数据来源方面,本研究中多数为单中心病例对照设计,利用ICU记录的回顾性数据建立模型,此类数据易于获取和使用,但该设计在预测因子和研究结局之间的时序关系方面易产生偏倚[33],PROBAST推荐诊断模型采用队列研究或巢式病例对照以减少选择偏倚[10]。另外,近半数研究EPV<20,样本量是构建稳定模型的前提,因此需要整合资源、扩大样本量。在研究实施阶段,部分研究仅运用单因素分析筛选预测因子,根据其统计学意义(如P<0.05)进行选择,并未与其他变量结合进行分析,而其中一些变量间存在交互作用,导致重要变量的遗失,由此产生偏倚[11]。逐步回归可避免多重共线,LASSO回归可同时进行参数估计和变量选择[34],均可用于变量筛选。除了统计学角度,还应根据临床意义、测量的可及性和测量成本角度全面纳入预测因子。此外,实施阶段应注重盲法的使用与报告,如送检标本编码盲法[14]。最后,在统计分析阶段:①连续变量的处理。以包含次数最多的“ICU住院日数”这一连续变量为例,研究者根据变量分布的中位数或均值,选择的分类截点包括5 d[13]、21 d[16]、30 d[28]等。这种基于模型开发样本计算得出的截断值临床意义较小,变量在应用人群与开发人群中分布的不同导致模型的外推性不强。当必需将连续变量转化为分类变量操作时,应检验连续变量的非线性拟合或分类变量采用通用认可的标准定义、临床意义等[10]。②模型验证与呈现。全面报告区分度和校准度结果才能明确模型的预测性能,模型校准度应通过H-L检验和绘制校准图进行综合评价。内部验证可较为准确估计模型表现、调整过拟合情况,外部验证以增强模型的外推性。此外,模型的呈现形式一定程度上决定了模型的可操作性。随着信息技术的发展,预测模型从抽象的回归方程、简明的列线图到目前的评分系统或APP计算器、动态列线图[35],模型更加直观,便于临床实际应用和模型的后续更新。
相对而言,Wang等[19]的研究质量较高,该模型基于AIC准则、使用向后逐步回归筛选预测因子,运用LR构建模型,采用蒙特卡洛多重插补处理缺失数据。模型区分度良好,决策曲线显示阈值概率在30%~95%范围内时,具有较高的净获益值,表明该模型临床预测效用良好。除此之外,Çaǧlayan等[21]运用机器学习方法代替传统回归,利用新算法挖掘4 503份电子病历数据、分析潜在预测因子,将防控关口前移预测ICU入院48 h内患者MDRO感染风险;Seo等[25]针对二级医院开发预测模型,以缩小不同等级医院防控差距;研究[22, 26]结合不同地区MDRO感染的流行病学,分别重点关注CRO、CRKP,以实现针对性的感控干预,以上模型从防控新视角、建模新方法为未来模型研究提供了新思路。
模型预测效能受到诸多因素的影响,且样本量要求较大,目前还没有普适性的ICU MDRO感染理想预测模型。虽然随着医院信息化系统的推广和新的统计学方法发展,如机器学习算法对电子病历系统所生成的庞大数据进行挖掘,可以进一步扩大样本量构建预测模型,但模型的效能不仅取决于其统计学特性,还取决于其使用背景[36]。从本研究结果来看,由于研究设计的局限性和研究人群的不同等问题,在决定如何在临床实践中使用这些模型时必须考虑到这些差异。因此,需要在当地环境中进行进一步的外部验证,以证实模型在临床决策支持中的有效性。
本研究也存在部分局限性:第一,研究只纳入了中英文文献,可能存在选择性偏倚;其次,由于研究对象和结局等方面的异质性,未对纳入文献进行整合和定量分析。
本研究共纳入17个ICU MDRO感染风险预测模型的研究,系统评价了模型的多方面特征。研究结果提示相关模型的研究还处在发展阶段,模型偏倚风险普遍较高、研究方法学细节和报告事项仍需研究者注意。建立基于多中心、大样本量数据的ICU MDRO风险预测模型,引入电子病历医疗大数据信息、充分利用最新算法构建模型,以及前瞻性地验证性能及更新模型,从而进一步将模型推广使用,发挥模型临床效能,可成为该领域的后续研究方向。医务人员应综合考虑模型的预测性能、预测因子的可获得性、结局测量的方便性、模型适用对象,以及应结合不同地区流行病学、不同等级医院医疗资源分布差异,选择适当的模型供临床使用,实现模型的推广应用价值。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Thangaraju P, Venkatesan S. WHO ten threats to global health in 2019:antimicrobial resistance[J]. Cukurova Med J, 2019, 44(3): 1150-1151. |
| [2] |
凌玲, 吴伟旋, 孙树梅, 等. 多重耐药菌医院感染直接经济负担的系统评价[J]. 中国感染控制杂志, 2017, 16(7): 616-621. Ling L, Wu WX, Sun SM, et al. Systematic evaluation on direct economic burden of healthcare-associated infection due to multidrug-resistant organisms[J]. Chinese Journal of Infection Control, 2017, 16(7): 616-621. DOI:10.3969/j.issn.1671-9638.2017.07.006 |
| [3] |
中国人大网. 中华人民共和国生物安全法[EB/OL]. (2020-10-17)[2022-07-29]. http://www.npc.gov.cn/npc/c30834/202010/bb3bee5122854893a69acf4005a66059.shtml. The National People's Congress of the People's Republic of China. Biological safety law of the People's Republic of China[EB/OL]. (2020-10-17)[2022-07-29]. http://www.npc.gov.cn/npc/c30834/202010/bb3bee5122854893a69acf4005a66059.shtml. |
| [4] |
刘阳, 吴明华, 令娟, 等. 重症监护病房多重耐药菌感染患者疾病谱分析[J]. 中国感染控制杂志, 2022, 21(3): 273-279. Liu Y, Wu MH, Ling J, et al. Disease spectrum of patients with multidrug-resistant organism infection in intensive care unit[J]. Chinese Journal of Infection Control, 2022, 21(3): 273-279. |
| [5] |
迟星云, 朱晓莉, 王虹, 等. 重症监护病房多重耐药菌检出及药物敏感性[J]. 中华医院感染学杂志, 2019, 29(24): 3729-3733. Chi XY, Zhu XL, Wang H, et al. Comparison of multi-drug resistant bacteria and drug sensitivity in intensive care unit[J]. Chinese Journal of Nosocomiology, 2019, 29(24): 3729-3733. |
| [6] |
杨启文, 吴安华, 胡必杰, 等. 临床重要耐药菌感染传播防控策略专家共识[J]. 中国感染控制杂志, 2021, 20(1): 1-14. Yang QW, Wu AH, Hu BJ, et al. Expert consensus on strategies for the prevention and control of spread of clinically important antimicrobial-resistant organisms[J]. Chinese Journal of Infection Control, 2021, 20(1): 1-14. |
| [7] |
Robotham JV, Deeny SR, Fuller C, et al. Cost-effectiveness of national mandatory screening of all admissions to English National Health Service hospitals for meticillin-resistant Staphylococcus aureus: a mathematical modelling study[J]. Lancet Infect Dis, 2016, 16(3): 348-356. DOI:10.1016/S1473-3099(15)00417-X |
| [8] |
陈玉, 张朝辉, 樊发超. 应用主动筛查预防与控制重症监护病房患者多重耐药菌感染[J]. 中国感染控制杂志, 2022, 21(2): 190-195. Chen Y, Zhang CH, Fan FC. Application of active screening to prevent and control multidrug-resistant organism infection in patients in intensive care unit[J]. Chinese Journal of Infection Control, 2022, 21(2): 190-195. |
| [9] |
Moons KGM, de Groot JAH, Bouwmeester W, et al. Critical appraisal and data extraction for systematic reviews of prediction modelling studies: the CHARMS checklist[J]. PLoS Med, 2014, 11(10): e1001744. DOI:10.1371/journal.pmed.1001744 |
| [10] |
Wolff RF, Moons KGM, Riley RD, et al. PROBAST: A tool to assess the risk of bias and applicability of prediction model studies[J]. Ann Intern Med, 2019, 170(1): 51-58. DOI:10.7326/M18-1376 |
| [11] |
陈香萍, 张奕, 庄一渝, 等. PROBAST: 诊断或预后多因素预测模型研究偏倚风险的评估工具[J]. 中国循证医学杂志, 2020, 20(6): 737-744. Chen XP, Zhang Y, Zhuang YY, et al. PROBAST: a tool for assessing risk of bias in the study of diagnostic or prognostic multi-factorial predictive models[J]. Chinese Journal of Evidence-Based Medicine, 2020, 20(6): 737-744. |
| [12] |
Mora-Jiménez I, Tarancón-Rey J, álvarez-Rodríguez J, et al. Artificial intelligence to get insights of multi-drug resistance risk factors during the first 48 hours from ICU admission[J]. Antibiotics (Basel), 2021, 10(3): 239. DOI:10.3390/antibiotics10030239 |
| [13] |
Vasudevan A, Mukhopadhyay A, Li JL, et al. A prediction tool for nosocomial multi-drug resistant Gram-negative bacilli infections in critically ill patients-prospective observational study[J]. BMC Infect Dis, 2014, 14: 615. DOI:10.1186/s12879-014-0615-z |
| [14] |
陈琛. ICU患者多重耐药菌感染危险因素及预测模型研究[D]. 银川: 宁夏医科大学, 2021. Chen C. Study on risk factors and prediction model of multi-drug resistant bacteria infection in ICU patients[D]. Yinchuan: Ningxia Medical University, 2021. |
| [15] |
项彦斌, 周燕, 杜建成, 等. 重症患者多重耐药菌感染的影响因素及预测模型分析[J]. 重庆医学, 2020, 49(23): 3966-3970. Xiang YB, Zhou Y, Du JC, et al. Influcing factors and prediction model of multidrug-resistant bacterial infection in severe patients[J]. Chongqing Medicine, 2020, 49(23): 3966-3970. DOI:10.3969/j.issn.1671-8348.2020.23.024 |
| [16] |
丁梦媛, 李文进, 耿苗苗, 等. 综合重症监护病房患者多重耐药菌医院感染风险评估模型构建[J]. 中国卫生资源, 2020, 23(4): 384-387, 399. Ding MY, Li WJ, Geng MM, et al. Risk assessment model construction of nosocomial infection of multi-drug resistant organism in comprehensive intensive care unit patients[J]. Chinese Health Resources, 2020, 23(4): 384-387, 399. DOI:10.3969/j.issn.1007-953X.2020.04.015 |
| [17] |
李娇, 商临萍, 郭红菊, 等. 综合ICU多重耐药菌医院感染的风险模型构建[J]. 中国感染控制杂志, 2016, 15(10): 730-734. Li J, Shang LP, Guo HJ, et al. Construction of risk model for healthcare-associated infection with multidrug-resistant organi-sms in general intensive care unit[J]. Chinese Journal of Infection Control, 2016, 15(10): 730-734. DOI:10.3969/j.issn.1671-9638.2016.10.003 |
| [18] |
Song JY, Jeong IS. Development of a risk prediction model of carbapenem-resistant Enterobacteriaceae colonization among patients in intensive care units[J]. Am J Infect Control, 2018, 46(11): 1240-1244. DOI:10.1016/j.ajic.2018.05.001 |
| [19] |
Wang L, Huang XL, Zhou JT, et al. Predicting the occurrence of multidrug-resistant organism colonization or infection in ICU patients: development and validation of a novel multiva-riate prediction model[J]. Antimicrob Resist Infect Control, 2020, 9(1): 66. DOI:10.1186/s13756-020-00726-5 |
| [20] |
昂慧. 重症监护室多重耐药菌感染的现状调查和危险因素的Logistic回归分析[D]. 荆州: 长江大学, 2018. Ang H. Investigation of multi-drug resistant organism in intensive care units and logistic analysis of risk factors[D]. Jingzhou: Yangtze University, 2018. |
| [21] |
Çaǧlayan Ç, Barnes SL, Pineles LL, et al. A data-driven framework for identifying intensive care unit admissions colonized with multidrug-resistant organisms[J]. Front Public Health, 2022, 10: 853757. DOI:10.3389/fpubh.2022.853757 |
| [22] |
Dantas LF, Dalmas B, Andrade RM, et al. Predicting acquisition of carbapenem-resistant Gram-negative pathogens in intensive care units[J]. J Hosp Infect, 2019, 103(2): 121-127. DOI:10.1016/j.jhin.2019.04.013 |
| [23] |
陈慧兰, 游秋萍, 孙萍. ICU多重耐药菌感染的护理防控要点与传播的预警模式构建[J]. 医学食疗与健康, 2021, 19(11): 96-97, 99. Chen HL, You QP, Sun P. Essentials of nursing prevention and control of multidrug-resistant bacteria infection in ICU and construction of early warning model of transmission[J]. Medical Diet and Health, 2021, 19(11): 96-97, 99. |
| [24] |
邹倩, 丁梦媛, 耿苗苗, 等. ICU多重耐药菌感染判别分析预判模型建立研究[J]. 医学研究杂志, 2021, 50(1): 32-36. Zou Q, Ding MY, Geng MM, et al. A discriminant model for early detection of patients with multidrug-resistant organisms in intensive care unit[J]. Journal of Medical Research, 2021, 50(1): 32-36. |
| [25] |
Seo SM, Jeong IS, Song JY, et al. Development of a nomogram for carbapenem-resistant Enterobacteriaceae acquisition risk prediction among patients in the intensive care unit of a secondary referral hospital[J]. Asian Nurs Res (Korean Soc Nurs Sci), 2021, 15(3): 174-180. |
| [26] |
Yang D, Xie ZQ, Xin XL, et al. A model for predicting nosocomial carbapenem-resistant Klebsiella pneumoniae infection[J]. Biomed Rep, 2016, 5(4): 501-505. |
| [27] |
李娜, 田永明, 唐志红. 多重耐药鲍曼不动杆菌医院感染危险因素预测模型构建[J]. 成都医学院学报, 2019, 14(6): 727-731, 735. Li N, Tian YM, Tang ZH. Construction of the predictive model for the risk factors of nosocomial infection with multi-drug resistant Acinetobacter baumannii[J]. Journal of Chengdu Medical College, 2019, 14(6): 727-731, 735. |
| [28] |
刘卫平, 李昊雪, 郭天慧, 等. 重症监护病房患者耐碳青霉烯类肠杆菌感染风险预测模型的建立与效果评价[J]. 中国消毒学杂志, 2022, 39(2): 135-137, 142. Liu WP, Li HX, Guo TH, et al. Establishment of risk prediction model for carbapenem resistant Enterobacteriaceae infection in intensive care unit and evaluation of effection[J]. Chinese Journal of Disinfection, 2022, 39(2): 135-137, 142. |
| [29] |
Vincent JL, Sakr Y, Singer M, et al. Prevalence and outcomes of infection among patients in intensive care units in 2017[J]. JAMA, 2020, 323(15): 1478-1487. |
| [30] |
邹倩, 耿苗苗, 祝延红. 基于循证理论构建重症监护病房患者多重耐药菌感染风险预测模型及外部验证研究[J]. 中国全科医学, 2022, 25(12): 1441-1448. Zou Q, Geng MM, Zhu YH. Development and external validation of an evidence-based risk prediction model for multidrug-resistant bacterial infections in ICU patients[J]. Chinese General Practice, 2022, 25(12): 1441-1448. |
| [31] |
Papp-Wallace KM, Endimiani A, Taracila MA, et al. Carbapenems: past, present, and future[J]. Antimicrob Agents Chemother, 2011, 55(11): 4943-4960. |
| [32] |
耿苗苗, 费凯虹, 邹倩, 等. 风险预判与主动干预在综合ICU患者多重耐药菌医院感染防控中的关键作用研究[J]. 现代生物医学进展, 2022, 22(2): 249-253. Geng MM, Fei KH, Zou Q, et al. The effect of risk prediction and active intervention on the control of healthcare associated infection caused by multi-drug resistant organism in GICU[J]. Progress in Modern Biomedicine, 2022, 22(2): 249-253. |
| [33] |
贺冰洁, 陈暐烨, 刘立立, 等. 宫颈癌发病风险预测模型的系统综述[J]. 中华流行病学杂志, 2021, 42(10): 1855-1862. He BJ, Chen WY, Liu LL, et al. The risk prediction models for occurrence of cervical cancer: a systematic review[J]. Chinese Journal of Epidemiology, 2021, 42(10): 1855-1862. |
| [34] |
张秀秀, 王慧, 田双双, 等. 高维数据回归分析中基于LASSO的自变量选择[J]. 中国卫生统计, 2013, 30(6): 922-926. Zhang XX, Wang H, Tian SS, et al. LASSO-based indepen-dent variable selection in high-dimensional data regression analysis[J]. Chinese Journal of Health Statistics, 2013, 30(6): 922-926. |
| [35] |
Jalali A, Alvarez-Iglesias A, Roshan D, et al. Visualising statistical models using dynamic nomograms[J]. PLoS One, 2019, 14(11): e0225253. |
| [36] |
Dent THS, Wright CF, Stephan BCM, et al. Risk prediction models: a framework for assessment[J]. Public Health Genomics, 2012, 15(2): 98-105. |



