2. 河北北方学院医学检验学院,河北 张家口 075000;
3. 承德医学院附属医院检验科,河北 承德 067000
 唑和红霉素的敏感率分别为97.8%、98.6%、98.0%、98.4%和96.3%。结论 2013—2022年河北省临床分离的单核细胞增生李斯特菌大多来源于血标本,感染人群以青年和新生儿为主,该菌已出现一线治疗药物的非敏感株,需持续关注。
唑和红霉素的敏感率分别为97.8%、98.6%、98.0%、98.4%和96.3%。结论 2013—2022年河北省临床分离的单核细胞增生李斯特菌大多来源于血标本,感染人群以青年和新生儿为主,该菌已出现一线治疗药物的非敏感株,需持续关注。2. College Lab Medicine, Hebei North University, Zhangjiakou 075000, China;
3. Department of Laboratory Medicine, Affiliated Hospital of Chengde Medical University, Chengde 067000, China
单核细胞增生李斯特菌(Listeria monocytogenes)为革兰阳性短小杆菌,不产芽孢,是一种人畜共患的病原菌,也是重要的食源性病原菌。其致病性强,老年人、孕妇、新生儿和免疫力低下者易感,感染后主要引起脑膜炎、菌血症、肺炎、急性胃肠炎和流产等疾病,临床表现缺少特异性。单核细胞增生李斯特菌感染病死率较高,可达30%~50%[1-2]。美国疾病控制与预防中心(CDC)报告[3]显示,美国每年约1 600人感染单核细胞增生李斯特菌,造成约260人死亡。我国报道病例多为孕妇与新生儿。一项研究[4]汇总我国2000—2009年16个省报告的92例单核细胞增生李斯特菌感染病例,病死率达21%,其中新生儿的病死率高达56%。由于临床分离率较低,目前我国针对单核细胞增生李斯特菌的大规模研究相对较少,检出情况及耐药状况尚未明确。因此,为了解河北省单核细胞增生李斯特菌临床分布特征及耐药情况,本研究对2013年1月—2022年6月河北省细菌耐药监测网75所医院的单核细胞增生李斯特菌的临床情况进行回顾性分析,为临床治疗和感染控制提供参考。
1 资料与方法 1.1 菌株数据来源收集2013年1月—2022年6月河北省细菌耐药监测网75所成员单位(包括32所二级医院,43所三级医院)检出的单核细胞增生李斯特菌菌株数据,剔除同一患者分离的重复菌株后纳入分析。
1.2 细菌鉴定及药敏试验75所医院进行细菌鉴定及药敏试验使用的仪器包括:VITEK 2 (bioMérieux, France)、Phoenix 100(Becton Dickinson and Company, America)、MALDI-TOF(Bruker Corporation, Germany)等。使用全自动微生物鉴定系统鉴定细菌至种。按照美国临床实验室标准化协会(CLSI)M45要求进行药敏试验及质控,药敏试验所用培养基为添加2.5%~5.0%裂解马血的阳离子调节的MH培养基,质控菌株为肺炎链球菌ATCC 49619,结果判读标准参照CLSI M45、欧洲抗菌药物敏感性试验委员会(EUCAST)执行[5-6],判读标准为菌株的最小抑菌浓度(MIC)值大于折点值为耐药或非敏感,小于折点值为敏感。
1.3 年龄分组参照全国细菌耐药监测网(China Antimicrobial Resistance Surveillance System,CARSS)分组标准[7]和国际标准年龄分类临时指南[8],将患者分为新生儿(≤28 d)、儿童(29 d~14岁)、青年(15~47岁)、中年(48~64岁)、老年(≥65岁)五个年龄组分别进行统计分析。
1.4 统计学分析应用WHONET 5.6软件和EXCEL进行数据整理、分析和绘图。
2 结果 2.1 单核细胞增生李斯特菌的时间分布2013年1月—2022年6月河北省检出单核细胞增生李斯特菌共187株,其中,男性检出70株,女性检出117株。2013年检出数量最少(4株),2021年检出数量最多(36株),大体呈增长趋势,见图 1。
 |
| 图 1 2013年1月—2022年6月河北省检出单核细胞增生李斯特菌的时间分布 Figure 1 Temporal distribution of L. monocytogenes isolated in Hebei Province from January 2013 to June 2022 |
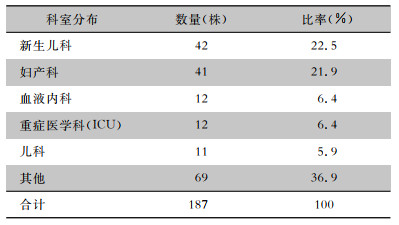
检出菌株数量居前三位的科室依次为新生儿科(22.5%)、妇产科(21.9%)和血液内科(6.4%)。科室分布见表 1。
| 表 1 2013年1月—2022年6月河北省单核细胞增生李斯特菌的科室分布 Table 1 Department distribution of L. monocytogenes isolated in Hebei Province from January 2013 to June 2022 |
|
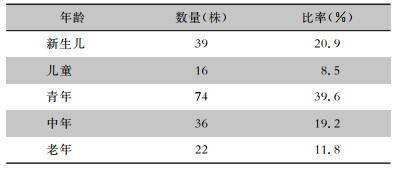
检出单核细胞增生李斯特菌数量居前三位的年龄组是青年(74株)、新生儿(39株)和中年(36株)人群,分别占39.6%、20.9%和19.2%,见表 2。
| 表 2 2013年1月—2022年6月河北省检出单核细胞增生李斯特菌的患者年龄分布 Table 2 Patient's age distribution of L. monocytogenes isolated in Hebei Province from January 2013 to June 2022 |
|
检出菌株数量居前三位的标本分别是血(129株)、脑脊液(20株)和胃液(14株),分别占69.0%、10.7%和7.5%,其他标本占比较少,见表 3。
| 表 3 2013年1月—2022年6月河北省单核细胞增生李斯特菌的标本来源分布 Table 3 Specimen source distribution of L. monocytogenes isolated in Hebei Province from January 2013 to June 2022 |

|
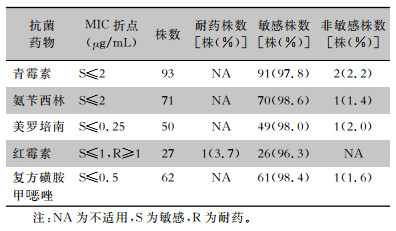
检出菌株对青霉素、氨苄西林、美罗培南、红霉素和复方磺胺甲

| 表 4 2013年1月—2022年6月河北省单核细胞增生李斯特菌药敏结果 Table 4 Antimicrobial susceptibility test results of L. monocytogenes isolated in Hebei Province from January 2013 to June 2022 |
|
本研究显示,2013年1月—2022年6月河北省单核细胞增生李斯特菌检出数整体呈上升趋势,与国内、外研究[9-10]一致,上升原因与临床感染增加有关,还是与近年临床和实验室对该菌的重视度提高有关,尚需进一步研究。同时,仍需密切关注单核细胞增生李斯特菌的感染和检出情况,并进行持续监测。
科室分布的结果显示,新生儿科和妇产科检出单核细胞增生李斯特菌比例较高,共83株,占总体的44.4%;年龄分布结果显示,青年和新生儿检出比例较高,共113株,占总体的60.4%。文献[4]指出,2000—2009年我国共报道92例李斯特菌病例,其中孕妇和新生儿占总数的58.6%。我国食源性疾病监测显示,2016年我国李斯特菌病主要以新生儿和孕妇为主[8],提示新生儿和孕妇可能为单核细胞增生李斯特菌的易感人群。李斯特菌为胞内寄生菌,致病物质主要是溶血素和菌体表面成分,细胞免疫是人体自我治愈李斯特菌病的重要机制[4]。新生儿细胞免疫能力有限,而孕妇黄酮素升高时,细胞免疫能力下降[11],因此,这些可能是新生儿和孕妇容易感染李斯特菌的部分原因。此外,单核细胞增生李斯特菌也可穿透胎盘内皮细胞层感染胎儿[12]。单核细胞增生李斯特菌容易存在于香肠类、生食蔬菜沙拉、冰激凌、未煮熟的鱼、巴氏杀菌牛奶和奶酪等食物中[13],因此,孕期应减少冷藏、冷冻食品的直接摄入,加强孕妇和新生儿单核细胞增生李斯特菌的检测,以预防该菌感染。
单核细胞增生李斯特菌检出率居前三位的标本为血、脑脊液和胃液,这符合单核细胞增生李斯特菌感染引起菌血症、中枢神经系统感染和发热性胃肠炎的特征[14],与郝民等[3]研究结果基本一致,血(13/28,46.4%)、胎盘(8/28,28.6%)和脑脊液(4/28,14.3%)为单核细胞增生李斯特菌前三位的标本来源。1964—2013年感染该菌的新生儿病死率高达52.6%(40/76),血流感染后病死率为28.6%(24/84),中枢神经系统感染病死率为39.1%(36/92)[15]。因此,临床需要提高对该菌的重视程度,尽早筛查;同时也要提升实验室对该菌的检测能力,提供快速准确的检测结果,有助于降低该菌感染的病死率。
单核细胞增生李斯特菌对头孢类抗生素天然耐药[16],能够用于该菌感染治疗的药物有限。因此,准确检测该菌的药敏结果至关重要。由于氨苄西林能穿透细胞膜,而青霉素类抗生素可以在细胞内稳定存在,因此,氨苄西林和青霉素对该菌杀伤性较强,治疗效果较好[17-18],常被用作治疗该菌所致感染的一线药物。本研究对2013年1月—2022年6月的耐药监测数据分析显示,该菌已经出现对青霉素、氨苄西林、美罗培南和复方磺胺甲


本研究数据来自多中心、长周期的观察结果,稳定可靠,对监测河北省单核细胞增生李斯特菌的特征有重要作用;但主要使用省内监测数据,且未能收集耐药菌株进行深入研究,具有一定局限性。
综上所述,2013—2022年河北省单核细胞增生李斯特菌主要分离人群为青年和新生儿,主要来自于血和脑脊液标本。虽然河北省抗菌药物使用逐渐规范化,但单核细胞增生李斯特菌仍然出现了非敏感菌株,因此,应持续监测该菌耐药性,并多中心收集非敏感菌株,深入探究其耐药机制,以指导临床预防和治疗。
利益冲突:所有作者均声明不存在利益冲突。
| [1] |
Chen JQ, Healey S, Regan P, et al. PCR-based methodologies for detection and characterization of Listeria monocytogenes and Listeria ivanovii in foods and environmental sources[J]. Food Sci Hum Wellness, 2017, 6(2): 39-59. DOI:10.1016/j.fshw.2017.03.001 |
| [2] |
Carroll KC, Pfaller MA, Landry ML, et al. Manual of clinical microbiology[M]. 12th ed. Washington, DC: ASM Press, 2019.
|
| [3] |
郝民, 阮明捷, 王恒伟, 等. 北京市朝阳区单核细胞增生李斯特菌关键毒力基因缺失与致病性关联性研究[J]. 中国食品卫生杂志, 2022, 34(1): 75-81. Hao M, Ruan MJ, Wang HW, et al. Study of association between deletion of key virulence genes and pathogenicity of Listeria monocytogenes in Chaoyang District of Beijing[J]. Chinese Journal of Food Hygiene, 2022, 34(1): 75-81. |
| [4] |
冯延芳, 冉陆, 张立实. 2000—2009年中国李斯特菌病文献报告病例分析[J]. 疾病监测, 2011, 26(8): 654-659. Feng YF, Ran L, Zhang LS. Listeriosis cases reported in medical literatures in China, 2000-2009[J]. Disease Surveillance, 2011, 26(8): 654-659. DOI:10.3784/j.issn.1003-9961.2011.08.021 |
| [5] |
Clinical and Laboratory Standards Institute. M45: methods for antimicrobial dilution and disk susceptibility testing of infrequently isolated or fastidious bacteria[EB/OL]. (2016-08-15)[2022-11-26]https://webstore.ansi.org/preview-pages/CLSI/preview_CLSI+M45-Ed3.pdf.
|
| [6] |
The European Committee on Antimicrobial Susceptibility Testing. Clinical breakpoints-breakpoints and guidance[EB/OL]. (2023-01-21)[2023-02-03]. https://www.eucast.org/clinical_breakpoints/
|
| [7] |
全国细菌耐药监测网. 2020年全国细菌耐药监测报告[J]. 中华检验医学杂志, 2022, 45(2): 122-136. China Antimicrobial Resistance Surveillance System. 2020 National antimicrobial resistance surveillance report[J]. Chinese Journal of Laboratory Medicine, 2022, 45(2): 122-136. |
| [8] |
Department of International Economic and Social Affairs. Provisional guidelines on standard international age classifications: ST/ESA/STAT/SEA. M/74[S]. New York: United Nations Publication, 1982.
|
| [9] |
McCollum JT, Cronquist AB, Silk BJ, et al. Multistate outbreak of listeriosis associated with cantaloupe[J]. N Engl J Med, 2013, 369(10): 944-953. DOI:10.1056/NEJMoa1215837 |
| [10] |
陈伟伟, 吴晓敏, 廖冬冬, 等. 2016年福建省单核细胞增生李斯特菌临床病例及食品来源菌株的分子特征分析[J]. 中国人兽共患病学报, 2019, 35(2): 145-148. Chen WW, Wu XM, Liao DD, et al. Molecular type analysis of Listeria monocytogenes stains isolated from clinical cases and food source in Fujian, China, 2016[J]. Chinese Journal of Zoonoses, 2019, 35(2): 145-148. |
| [11] |
Leber A, Zenclussen ML, Teles A, et al. Pregnancy: tole-rance and suppression of immune responses[J]. Methods Mol Biol, 2011, 677: 397-417. |
| [12] |
Naruse K, Yamasaki M, Harada N, et al. Maternal listeriosis in pregnancy associated with measles virus infection[J]. J Obstet Gynaecol Res, 2004, 30(2): 117-119. DOI:10.1111/j.1447-0756.2003.00170.x |
| [13] |
宋筱瑜, 裴晓燕, 徐海滨, 等. 我国零售食品单增李斯特菌污染的健康风险分级研究[J]. 中国食品卫生杂志, 2015, 27(4): 447-450. Song XY, Pei XY, Xu HB, et al. Risk ranking of Listeria monocytogenes contaminated ready-to-eat foods at retail for sensitive population in China[J]. Chinese Journal of Food Hygiene, 2015, 27(4): 447-450. |
| [14] |
Zhu Q, Gooneratne R, Hussain MA. Listeria monocytogenes in fresh produce: outbreaks, prevalence and contamination levels[J]. Foods, 2017, 6(3): 21. DOI:10.3390/foods6030021 |
| [15] |
孙照琨, 吴璇, 陈蕊, 等. 李斯特菌病既往中国文献报告病例分析[J]. 中国微生态学杂志, 2016, 28(11): 1323-1326. Sun ZK, Wu X, Chen R, et al. Previous cases of Listeria disease reported in China[J]. Chinese Journal of Microecology, 2016, 28(11): 1323-1326. |
| [16] |
周文莉, 朱敏丽, 严超英, 等. 新生儿单核细胞增多性李斯特菌感染7例[J]. 中国当代儿科杂志, 2010, 12(2): 154-155. Zhou WL, Zhu ML, Yan CY, et al. Neonatal sepsis caused by Listeria monocytogenes: case report of 7 cases[J]. Chinese Journal of Contemporary Pediatrics, 2010, 12(2): 154-155. |
| [17] |
丁子俊, 张新华. 新生儿单核细胞增生性李斯特菌脑膜炎的临床特征及药敏分析[J]. 中国药物与临床, 2019, 19(18): 3164-3166. Ding ZJ, Zhang XH. Clinical characteristics and drug sensitivity analysis of neonatal Listeria monocytogenes meningitis[J]. Chinese Remedies & Clinics, 2019, 19(18): 3164-3166. |
| [18] |
Kylat RI, Bartholomew A, Cramer N, et al. Neonatal listeriosis: Uncommon or misdiagnosed?[J]. J Neonatal Perinatal Med, 2016, 9(3): 313-316. |
| [19] |
杨梅, 王志刚, 封志纯, 等. 单核细胞增生性李斯特菌感染临床特征及耐药性[J]. 中华实用儿科临床杂志, 2014, 29(22): 1692-1695. Yang M, Wang ZG, Feng ZC, et al. Clinical features and drug resistance of Listeria monocytogenes infection in neonates[J]. Chinese Journal of Applied Clinical Pediatrics, 2014, 29(22): 1692-1695. |
| [20] |
潘冬妮, 解道敏. 新生儿李斯特菌感染15例临床探讨[J]. 中外医疗, 2018, 37(3): 84-85, 88. Pan DN, Xie DM. Clinical observation of 15 cases of neonatal Liszt rand infection[J]. China & Foreign Medical Treatment, 2018, 37(3): 84-85, 88. |
| [21] |
刘洋, 周厚德, 游兴勇, 等. 2016—2020年江西省市售熟肉制品中单增李斯特菌污染情况调查及耐药研究[J]. 现代预防医学, 2022, 49(2): 236-240. Liu Y, Zhou HD, You XY, et al. Investigation on contamination and drug resistance of Listeria monocytogenes levels from bulk cooked meats in Jiangxi Province from 2016 to 2020[J]. Modern Preventive Medicine, 2022, 49(2): 236-240. |
| [22] |
崔彦超, 李东, 夏丽娇. 临床分离单核细胞增生李斯特菌耐药情况分析[J]. 实用医技杂志, 2019, 26(5): 570-572. Cui YC, Li D, Xia LJ. Analysis of drug resistance of clinical isolates of Listeria monocytogenes[J]. Journal of Practical Medical Techniques, 2019, 26(5): 570-572. |



